INTRODUÇÃO
Recentes estudos têm demonstrado que a terapia de ressincronização cardíaca através da estimulação biventricular é um importante tratamento coadjuvante à terapia medicamentosa otimizada, em pacientes com insuficiência cardíaca congestiva (ICC) refratária, causada por disfunção ventricular esquerda crônica e distúrbios de condução intraventricular, promovendo melhora da função cardíaca e da qualidade de vida [1-3].
A técnica para a estimulação ventricular esquerda pode ser realizada tanto por modo epimiocárdico, através de toracotomia, como pode ser realizada através do epicárdio de maneira transvenosa. Visto que a última técnica é a de escolha, a maior limitação deste tratamento é a cateterização e inserção de eletrodo no seio coronário (SC) e suas tributárias para estimulação do ventrículo esquerdo [4].
O implante do eletrodo específico para estimulação ventricular esquerda é um procedimento relativamente complexo, que envolve as variações da anatomia das veias coronarianas, qualidade do material utilizado e experiência do cirurgião [5]. A impossibilidade de cateterização do SC, variações da anatomia do sistema venoso coronariano e estimulação diafragmática são as mais freqüentes causas de insucesso no posicionamento do eletrodo. A taxa de insucesso tende a cair com o aumento de variações nos modelos dos eletrodos e experiência do cirurgião [6-9].
Com os bons resultados apresentados com este tratamento coadjuvante, a terapia de ressincronização cardíaca vem se tornando um tratamento de rotina em pacientes previamente selecionados. Com o passar do tempo, em conseqüência da complexidade do procedimento, a comunidade de engenharia médica-científica vem investindo na adaptação de material para facilitar a técnica de implante [7,10,11].
O objetivo deste trabalho é apresentar a experiência de quatro anos, baseada em 157 procedimentos para a cateterização do seio coronariano realizado em pacientes previamente selecionados, submetidos à terapia de ressincronização cardíaca, utilizando uma técnica simplificada para cateterização do seio coronariano, por meio da anatomia radiológica e do eletrograma intracavitário, demonstrando a taxa de sucesso, complicações e tempo total de utilização de radioscopia.
MÉTODO
Caracterização do estudo
Trata-se de um estudo realizado no Serviço de Clínica e Cirurgia Cardiovascular Prof. Dr. Sérgio Almeida de Oliveira do Hospital Real e Benemérita Sociedade Portuguesa de Beneficência de São Paulo, sendo os dados colhidos de pacientes submetidos ao implante de marcapasso biventricular, no período compreendido entre outubro de 2001 e fevereiro de 2005. O estudo foi dividido em três fases de observação para a avaliação da taxa de sucesso e tempo de utilização de radioscopia. A primeira fase compreendida entre outubro de 2001 e setembro de 2002, a segunda, entre outubro de 2002 e setembro de 2003 e a terceira, de outubro de 2003 a fevereiro de 2005.
População
Foram estudados 157 pacientes com idades entre 26 e 84 anos, idade média de 55 ± 16 anos, 68 (43,5%) do sexo feminino e 89 (56,5%) do sexo masculino, portadores de cardiomiopatia dilatada. Quinze (9,8%) pacientes apresentavam fibrilação atrial permanente e 16 (10,5%) eram portadores de marcapasso definitivo previamente implantado para tratamento de bradiarritmias.
Critérios de inclusão
Foram considerados critérios de inclusão: 1) pacientes com cardiomiopatia dilatada (CMD) e insuficiência cardíaca congestiva classe funcional (NYHA) III ou IV refratária à terapia medicamentosa otimizada; 2) pacientes com CMD na qual não exista possibilidade de correção cirúrgica (revascularização do miocárdio, trocas valvares, ressecção de aneurisma ventricular esquerdo ou correção de cardiopatias congênitas); 3) pacientes sem indicação primária de restabelecimento da freqüência cardíaca e/ou do sincronismo atrioventricular; 4) distúrbio de condução interventricular exteriorizado sob a forma de padrão de bloqueio de ramo esquerdo, de ramo direito, associado ao bloqueio divisional ântero-superior ou de ramo esquerdo induzido por estimulação cardíaca ventricular direita exclusiva; 5) duração do complexo QRS maior ou igual a 130 ms.
Critérios de exclusão
1) infarto ou angina instável nos últimos três meses;
2) miocardite aguda;
3) gravidez e
4) abuso de drogas ou álcool.
Procedimento cirúrgico
Todos os procedimentos foram realizados sob anestesia local e, eventualmente, sob sedação, dependendo do grau da ICC e da tolerância ao tempo prolongado de decúbito. Os pacientes receberam antibiótico profilático intravenoso, uma hora antes do procedimento. Os pacientes foram colocados em decúbito dorsal horizontal, realizada a monitorização eletrocardiográfica com todos os eletrodos posicionados em hemi-tórax direito, quando a operação foi realizada do lado esquerdo (de escolha), ou esquerdo quando a operação foi realizada do lado direito (casos em que houve impossibilidade de implante do lado de preferência ou quando o paciente já era portador de marcapasso definitivo implantado à direita), de modo que todos ficassem afastados da silhueta cardíaca (dois eletrodos em região do deltóide direito: anterior e posterior) e um eletrodo em linha axilar anterior-esquerda no sétimo espaço intercostal. A derivação utilizada foi bipolar D2, sendo o eletrodo ativo sempre posicionado em região deltóide.
O primeiro eletrodo a ser posicionado foi o do ventrículo direito (VD), seguido pelo eletrodo de átrio direito, ambos, quando possível, pela veia cefálica esquerda. Quando não foi possível a passagem de um ou nenhum dos dois eletrodos, optava-se pela realização de nova punção venosa para obtenção da via de passagem. Estes eletrodos (fixação ativa) foram posicionados em locais tradicionais (eletrodo do átrio em aurícula direita e do ventrículo direito na ponta do mesmo) ou onde se obtivessem limiares de estimulação, de sensibilidade e impedância aceitáveis. Nos casos em que havia indicação de implante de cardioversor-desfibrilador implantável (CDI) concomitante, foi utilizado eletrodo dupla mola de fixação passiva, posicionado em ponta de ventrículo direito. Em portadores de marcapasso dupla câmara previamente implantado, foi realizada apenas uma punção para passagem do eletrodo de estimulação ventricular esquerda. O último eletrodo a ser posicionado foi o eletrodo do seio coronariano para estimulação de ventrículo esquerdo. Em nosso estudo, foram utilizados os eletrodos: Aescula 1055K (St Jude Medical), Attain 2187 ou 4193 (Medtronic) e Corox+ LV-H ou Corox OTW (Biotronik). O mesmo foi passado através de nova punção de veia subclávia e a cateterização do seio coronariano obtida pela utilização da anatomia radiológica com fluoroscopia em incidência oblíqua anterior esquerda, em um ângulo de 35 graus e eletrograma intracavitário unipolar obtido por conexão do eletrodo de seio coronariano com o eletrodo explorador da monitorização eletrocardiográfica (Figura 1).
O eletrodo foi adaptado de forma a respeitar a anatomia do átrio direito. Sua adaptação foi realizada pela formatação de suas guias (Figura 2).
Após sua formatação, o eletrodo foi posicionado em região de septo atrial baixo. Nesta posição, o eletrodo foi mobilizado suavemente em direções: superior, inferior (utilizando-se anatomia radiológica), anterior e posterior, através de rotação anti-horária e horária, respectivamente (utilizando-se eletrograma intracavitário). Regiões próximas ao anel atrioventricular exibiam eletrogramas bem definidos e com presença de componente atrial e ventricular.
Nos pacientes que apresentavam ritmo sinusal, o componente atrial na região do óstio do seio coronário apresentou-se isodifásico (Figura 3A). À medida que o eletrodo se posteriorizou, afastando-se do óstio do SC, o componente atrial tornou-se progressivamente mais negativo (Figura 3B) e, ao contrário, à medida que se anteriorizou, afastando-se do óstio, tornou-se progressivamente positivo (Figura 3C). Nesta situação, não era raro que atravessasse a valva tricúspide e migrasse para o ventrículo, gerando potenciais ventriculares de alta amplitude, induzindo, eventualmente, taquicardia ventricular não sustentada.
Sabe-se que o eletrograma intracavitário atrial direito apresenta diferentes morfologias e componentes que são dependentes do posicionamento do eletrodo em suas diferentes regiões anatômicas. Regiões de átrio direito alto apresentam potenciais predominantemente negativos, regiões de átrio direito médio apresentam potenciais isodifásicos e regiões de átrio direito baixo apresentam potenciais predominantemente positivos [12] (Figura 4A, B e C).
Após a cateterização do óstio do seio coronariano com o próprio eletrodo, o mesmo foi posicionado em veia tributária do seio coronariano, utilizando a formatação da própria guia utilizada para cateterização do óstio, ou em determinados casos uma nova guia formatada em "S" foi introduzida no eletrodo, facilitando o posicionamento nas mesmas. A escolha foi realizada dando-se preferência às veias da parede lateral e posterior do ventrículo esquerdo, seguido pela estabilidade do cateter, ausência de estimulação diafragmática com estimulação de energia máxima (10 Volts), limiares de estimulação sensibilidade e impedância de ventrículo esquerdo e biventricular, nos casos de geradores sem saída independente.
RESULTADOS
A estimulação ventricular esquerda foi obtida com sucesso em todos os pacientes. Em 11 pacientes não se obteve sucesso na estimulação ventricular esquerda por via transvenosa na primeira operação, seis por impossibilidade de cateterização do seio coronário e cinco por falha de posicionamento em uma das tributárias do seio venoso coronariano. Estes pacientes foram submetidos de imediato ao implante de eletrodo epimiocárdico por toracotomia. Cinco dos pacientes submetidos a implante de eletrodo epimiocárdico apresentaram, após um tempo médio de 29,4 ± 4,6 meses, aumento excessivo no limiar de comando do eletrodo para estimulação ventricular esquerda. Foram submetidos a uma reintervenção para nova tentativa de estimulação transvenosa, sendo que desta vez obteve-se sucesso nos cinco procedimentos (Figura 5).
A canulação do seio coronário com a utilização da anatomia radiológica e eletrograma intracavitário foi realizada com sucesso em 150 procedimentos. No momento da canulação do óstio de seio coronário em pacientes que se apresentavam em ritmo sinusal (136 pacientes), o componente atrial se mostrou isodifásico em 133 (97,7% dos pacientes em ritmo sinusal) e predominantemente positivo em três (2,3%) doentes. O posicionamento do eletrodo em tributárias do seio coronário foi obtido com sucesso em 145 (92,9%) procedimentos, com tempo médio de radioscopia de 18,27 ± 15,46 min. Com o treinamento do cirurgião, a taxa de sucesso progressivamente aumentou; na primeira fase de observação, esta foi de 55,5%, com tempo médio de radioscopia de 43,6 ± 18,6 min, na segunda, foi de 92,6%, com 18,14 ± 13 min e na terceira, foi de 98,2%, com tempo médio de 13,76 ± 4,66 min. Em cinco pacientes, nos quais foi obtida a canulação do seio coronário, não obtivemos sucesso no posicionamento do eletrodo: em quatro casos devido à dificuldade de posicionar o eletrodo em alguma tributária do sistema venoso coronariano e, conseqüentemente, impossibilidade de se obter limiares aceitáveis; em um paciente devido à estimulação diafragmática no único local em que era possível realizar a estimulação do ventrículo esquerdo. Em 11 procedimentos, a estimulação do ventrículo esquerdo foi obtida através de implante de eletrodo epimiocárdico por toracotomia.
Encontramos dificuldade de canulação do seio coronariano em 20 pacientes, apesar do adequados potenciais intracavitários e posicionamento anátomo-radiológico. Em seis casos, foram realizadas manobras com o eletrodo e o guia, que possibilitaram a passagem do eletrodo através do óstio, evidenciando posteriorização do seio coronário. Em oito casos, uma guia mais rígida e com curvatura mais acentuada foi utilizada, facilitando a passagem do eletrodo. Em 39 pacientes, tivemos dificuldade na progressão do eletrodo, aproximadamente, na provável região de drenagem da grande veia cardíaca no seio coronário. Este problema foi solucionado em 30 procedimentos através de sucessivas manipulações do eletrodo e seu guia. Em nove casos, a guia pré-formatada foi trocada por uma reta mais rígida. Em 12 casos, tivemos que reposicionar o eletrodo após a retirada da guia e desposicionamento acidental do mesmo. Dez pacientes apresentaram estimulação diafragmática, sendo o eletrodo reposicionado com sucesso em nove pacientes. Três pacientes apresentaram bloqueio atrioventricular total transitório após manipulação do eletrodo na cavidade ventricular direita, sendo necessária a estimulação ventricular provisória. Em três casos, houve deslocamento do eletrodo atrial durante a manipulação do eletrodo do seio coronário, necessitando seu reposicionamento.
Em dois casos, o implante do lado esquerdo foi interrompido e realizado do lado direito com sucesso; um por impossibilidade de se avançar os eletrodos para as cavidades direitas, devido à provável angulação na drenagem da veia inominada na veia cava superior, e o outro, devido à presença de veia cava esquerda persistente e seio coronário estreito, impossibilitando a passagem dos três eletrodos, pela mesma via de acesso.

Fig. 1 - Foto demonstrando o procedimento para obtenção de eletrograma intracavitário unipolar. Observe que o anel distal do eletrodo é conectado ao eletrodo explorador por meio de um fio de condução elétrica.

Fig. 2 - Guias com diferentes formatações (curvas com diferentes tamanhos e formas) para se adequar às variações em tamanho e anatomia dos átrios.
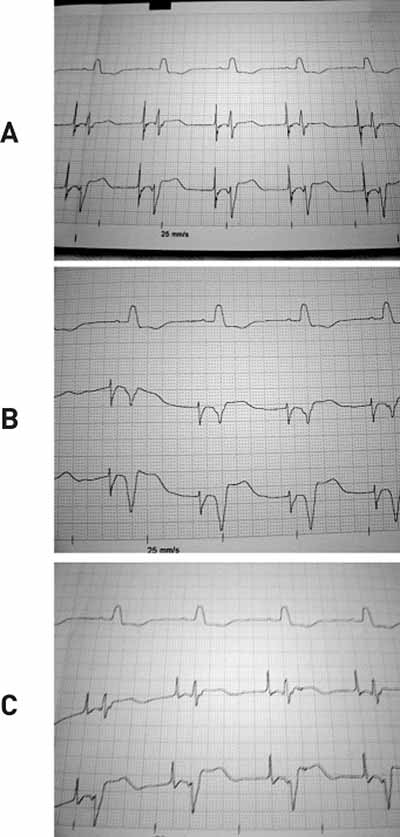
Fig. 3 - Registro com três traçados. O traçado superior evidenciando eletrocardiograma de superfície em 25 mm/s. Os traçados inferiores evidenciando eletrogramas intracavitários unipolares obtidos durante o procedimento, com o eletrodo posicionado em região pôstero-septal direita. (A) Eletrograma intracavitário obtido no óstio do seio coronário. (B) Eletrograma obtido, próximo, porém em regiões mais posteriores ao óstio do seio coronário. (C) Eletrograma obtido próximo, porém em regiões mais anteriores ao óstio do seio coronário.

Fig. 4 - Ilustração esquemática da cavidade atrial direita, demonstrando o posicionamento do eletrodo nas regiões alta, média e baixa do átrio direito e o vetor resultante da despolarização atrial direita. À esquerda a ilustração esquemática do eletrograma intracavitário obtido nas três situações. (A) Eletrodo posicionado na região mais posterior ao óstio do seio coronário (átrio direito alto). (B) Eletrodo posicionado em região do óstio do seio (átrio direito médio). (C) Eletrodo posicionado em região mais anterior ao seio do óstio coronário (átrio direito baixo). (SC=óstio do seio coronário, FO=fossa ovalis, VCI=veia cava inferior, VCS=veia cava superior, NAV=nodo átrio-ventricular, NSA=nodo sino-atrial, AD=átrio direito.
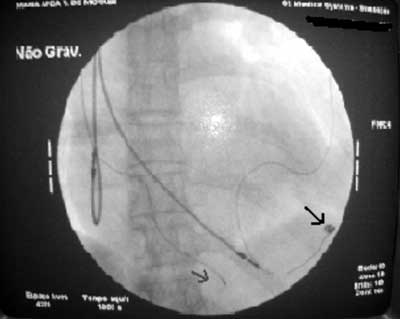
Fig. 5 - Imagem de radioscopia em posição oblíqua anterior esquerda de um paciente que foi submetido a uma re-intervenção para estimulação transvenosa do VE. Observe a seta escura mostrando eletrodo epicárdico abandonado, e a seta clara mostrando o eletrodo transvenoso posicionado em região posterior do ventrículo esquerdo.
COMENTÁRIOS
A terapia de ressincronização cardíaca tem mostrado bons resultados no tratamento de portadores de ICC previamente selecionados [1-3]. A rotina histórica de implante de eletrodo para estimulação ventricular esquerda tem sido sua fixação epimiocárdica sob visão direta por toracotomia lateral ou subxifoídea, ou por toracoscopia. Esses métodos já provaram serem eficazes e eram rotina antes da invenção dos eletrodos transvenosos para estimulação epicárdica, tendo como acesso a via endocárdica [13]. O maior obstáculo ao implante de rotina do eletrodo para estimulação ventricular esquerda, em portadores de cardiomiopatia dilatada e ICC, via epimiocárdica, são os riscos associados à anestesia geral e à morbidade pós-cirúrgica [14]. Atualmente, o método transvenoso por acesso endocárdico é o de escolha por reduzir a complexidade cirúrgica e, conseqüentemente, a sua morbidade e tempo de permanência hospitalar [7].
Uma das principais limitações da aplicação da técnica transvenosa é a cateterização do seio coronário e o posicionamento do eletrodo especial em uma de suas tributárias para estimulação ventricular esquerda [5,13]. O sucesso no implante depende de múltiplas variáveis, incluindo experiência e técnica do cirurgião, anatomia do seio coronariano, disponibilidade e variedade de material especial [6].
Apesar dos grandes avanços na tecnologia e evolução nas técnicas de implante com sistemas de bainha, sistemas especiais de guias, "side-the-wire" [11] e "over-the-wire" [8,13], ou propostas de canulação do seio coronário guiado por cateter eletrofisiológico [7] têm demonstrado serem eficazes. Porém, as técnicas propostas, sejam por meio de bainha associada ao contraste, guias especiais ou sinal elétrico intracavitário inadequado, ainda se utilizam apenas da anatomia radiológica e série de tentativas e erros para a canulação do seio coronário. Tendo em vista esta limitação ainda remanescente, os autores apresentam a experiência, em um único centro, de uma técnica que procura facilitar a canulação do seio coronário, baseada na anatomia radiológica e eletrograma intracavitário, dando ênfase à morfologia do eletrograma atrial nos pacientes que apresentam ritmo sinusal.
O procedimento foi realizado, preferencialmente, à esquerda por dois motivos. Primeiro, pela facilidade de tunelização do eletrodo para loja do marcapasso nos casos em que a estimulação tivesse que ser realizada via epimiocárdica, por toracotomia. O segundo é que, eventualmente, pacientes apresentam veia cava esquerda persistente com atresia de óstio de seio coronariano [14,15], impossibilitando o implante à direita. Optou-se por implantar os eletrodos convencionais para estimulação ventricular e atrial direitas, respectivamente, por servirem como pontos de definição anatômica e porque, durante a manipulação do eletrodo, nestes pacientes com bloqueio de ramo esquerdo, existe o risco de trauma do ramo direito, provocando bloqueio atrioventricular total e necessidade de estimulação cardíaca temporária, o que, assim como descrito na literatura [6], ocorreu em dois pacientes.
Com a utilização da radioscopia em incidência oblíqua anterior esquerda (OAE) a 35o, foi obtida a relação anatômica bidimensional do anel tricuspídeo e mitral, podendo-se evidenciar a parede lateral e septal do átrio direito. Com o auxílio do eletrograma intracavitário podemos identificar as regiões próximas ao anel atrioventricular, que demonstram eletrogramas intracavitários atriais e ventriculares com relação 1:2 ou menores [16]. Sabendo-se que o óstio do seio coronário se encontra na região póstero-septal direita, próximo, ou no próprio anel atrioventricular, o eletrodo foi posicionado nesta região, com utilização da guia do próprio eletrodo previamente formatada, observando-se a presença de eletrograma atrial e ventricular.
Manipulações para região superior e inferior foram facilmente realizadas utilizando-se anatomia radiológica. Porém, a radioscopia nos ofereceu imagens bidimensionais, conseqüentemente, mobilizações para regiões anteriores e posteriores não poderiam ser monitorizadas pela mesma. Desta maneira, estas manipulações do eletrodo foram acompanhadas com base no componente atrial do eletrograma intracavitário, em portadores de ritmo sinusal. Observou-se que, no óstio do seio coronariano, local a partir do qual foi possível a cateterização do seio coronário, o eletrograma intracavitário se mostrou isodifásico em 133 dos 136 procedimentos, nos quais os pacientes se encontravam em ritmo sinusal e foi possível a cateterização do seio coronariano. Nestes pacientes ainda observou-se que pequenas mobilizações do eletrodo para região posterior tornavam o componente atrial predominantemente negativo, e que mobilizações para região anterior o tornavam predominantemente positivo, posições que foram checadas com a radioscopia em incidência oblíqua anterior direita (OAD). Encontrou-se uma possível explicação para estas observações. Sabe-se que o vetor resultante da despolarização atrial direita tem início na região do nó sinusal, é direcionado para baixo, para frente e um pouco para esquerda [15,17].
Sabendo-se que o óstio do seio coronário se apresenta na região posterior do átrio direito, ântero-lateralmente à válvula da veia cava inferior e anteriormente relacionado à cúspide septal da valva tricúspide [18], o mesmo, devido a sua posição anatômica, ficaria perpendicular ao vetor de despolarização atrial. Tendo em vista que o eletrograma atrial obtido com o eletrodo é unipolar, o posicionamento deste sobre o óstio do seio coronário o colocaria em posição vertical de aproximadamente 90o, gerando potenciais isodifásicos [17]. Nesta situação, movimentando-se o eletrodo em direção posterior, o eletrodo tenderia a observar a cauda do vetor, tornando o sinal mais negativo e, ao contrário, em direção anterior, mais positivo, por observar a ponta do vetor [17], assim como demonstrado na Figura 4.
Galvão Filho [12], em 1990, também, demonstrou que o eletrograma atrial varia conforme sua localização no átrio direito. Porém, utilizou uma maneira diferente do autor de descrição anatômica do átrio direito, baseada em uma imagem bidimensional. O que Galvão Filho nomeou de átrio direito alto e átrio direito baixo correspondeu às regiões superior e "inferior" (próximas ao anel tricuspídeo) do átrio direito. Na anatomia radiológica utilizada pelos autores (incidência oblíqua anterior esquerda), regiões posteriores ao óstio do seio coronário corresponderam à região superior do átrio direito e regiões anteriores ao óstio do seio coronário corresponderam à região "inferior".
Nossa taxa de sucesso de 94,4%, semelhante a da literatura [6-8], com uma curva de aprendizado claramente evidenciada pelo porcentual de sucesso no primeiro ano de experiência de 55,5%, quando comparada ao último ano de 98,2%. O registro europeu do CONTAK revelou com detalhes que o tempo médio de duração do procedimento e a taxa de sucesso foi diretamente proporcional à experiência do cirurgião [8]. Cirurgiões com mais de 20 implantes de experiência obtiveram os menores tempos de procedimento, associados aos menores tempos de utilização de radioscopia para o implante. O tempo médio para o implante foi de 90 ± 38 min, com tempo de radioscopia de 27 ± 21 min. O nosso tempo médio de utilização total de radioscopia foi de 18,21 min. Comparado ao da literatura, nosso tempo médio total de radioscopia foi menor que o citado por Kautzner et al. [6], Butter et al. [10], Purerfellner et al. [7], Yee et al. [19]. Esta observação pode ser explicada pelo fato de que nestes trabalhos houve o envolvimento de muitos cirurgiões e, em alguns casos, de muitos centros, sendo que os resultados podem ter sido influenciados pela experiência de cada cirurgião. Neste trabalho, os resultados foram influenciados pela curva de aprendizado de um único cirurgião. Também neste não foi utilizada a bainha para cateterização do seio coronário, sendo o mesmo canulado diretamente com o próprio eletrodo, diminuindo, desta forma, as chances de deslocamento do mesmo com a retirada da bainha e conseqüente prolongamento no tempo do procedimento [4].
Analisando as dificuldades intra-operatórias, em 20 procedimentos encontramos dificuldade na canulação do óstio do seio coronário. Em seis procedimentos, não foi possível sua canulação e, em cinco pacientes, não foi possível o posicionamento do eletrodo em uma de suas tributárias, demonstrando a importância da variação anatômica do óstio do seio coronário que, eventualmente, pode se mostrar posteriorizado [6], da angulação e do calibre de suas tributárias, e mesmo a presença e anatomia da válvula de Thebésios, na cateterização do seio coronariano. Em um estudo de 143 pacientes estudados, 62,9% apresentavam a válvula, em 73 pacientes, a mesma apresentava formato semilunar, em 10 casos, forma de septo e, em sete, forma de crista [20]. Em 39 procedimentos, ocorreram dificuldades na progressão do eletrodo através do seio venoso coronariano, aproximadamente no local da drenagem da grande veia cardíaca, provável localização da válvula de Vissencius, encontrada em 87% dos casos estudados por Lundinghausen et al. [21], demonstrando, também, a importância da presença desta válvula no procedimento de implante do eletrodo do seio coronário.
CONCLUSÃO
A técnica de implante empregada pelo autor, utilizando eletrograma intracavitário e anatomia radiológica, demonstrou ser segura e eficaz para canulação do óstio do seio coronariano e posicionamento do mesmo em uma de suas tributárias, necessitando de reduzido tempo de radioscopia.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Aurichio A, Stellbrink C, Sack S et al. Chronic benefit as a result of pacing in congestive heart failure: results of the PATH-CHF trial. Circulation. 2000;102:3352A.
2. Linde C, Leclercq C, Rex S, Garrigue S, Lavergne T, Cazeau S et al. Long-term benefits of biventricular pacing in congestive heart failure: results from the MUltisite STimulation In Cardiomyopathy (MUSTIC) study. J Am Coll Cardiol. 2002;40(1):111-8.
3. Abraham WT, Fisher WG, Smith AL, Delurgio DB, Leon AR, Loh E et al. Cardiac resynchronization in chronic heart failure. N Engl J Med. 2002;346(24):1845-53.
4. Fatemi M, Etienne Y, Gilard M, Mansourati J, Blanc JJ. Short and long-term single-center experience with an S-shaped unipolar lead for left ventricular pacing. Europace. 2003;5(2):207-11.
5. Curnis A, Neris R, Mascioli G et al. Left ventricular pacing lead choice base on coronary sinus venous anatomy. Eur Heart J. 2000;2(Suppl J):J31-5.
6. Kautzner J, Riedlbauchová L, Cihák R, Bytesnic J, Vancura V. Technical aspects of implantation of LV lead for cardiac resynchronization therapy in chronic heart failure. Pacing Clin Electrophysiol. 2004;27(6 pt 1):783-90.
7. Purerfellner H, Nesser HJ, Winter S, Schwierz T, Hornell H, Maertens S. Transvenous left ventricular lead implantation with the EASYTRACK lead system: the European experience. Am J Cardiol. 2000;86(9 suppl 1):K157-64.
8. Neuzner J, Pappone C, Aurichio A et al. Learning curve for the first 1000 over-the-wire left ventricular transvenous lead implants-a Europe experience. Eur J Heart Failure 2001;3(suppl.1):S13.
9. Curley J, Lamba S, Moulton K et al. Does the availability of left heart lead and delivery system options matter for cardiac resynchronization therapy? Pacing Clin Electrophysiol. 2002;24(Pt. II):597.
10. Butter C, Gras D, Ritter P, Stellbrink C, Fleck E, Tockman B et al. Comparative prospective randomized efficacy testing of different guiding catheters for coronary sinus cannulation in heart failure patients. J Interv Card Electrophysiol. 2003;9(3):343-51.
11. Walker S, Levy T, Rex S, Paul VE. The use of a "side-wire" permanent transvenous-pacing electrode for left ventricular pacing. Europace. 1999;1(3):197-200.
12. Galvão Filho SS. Passagem de cabo eletrodo para estimulação cardíaca artificial provisória, orientada por monitorização endocavitária. An Paul Med Cir. 1990;117(1,2):47-53.
13. Auricchio A, Klein H, Tockman B, Sack S, Stellbrink C, Neuzner J et al. Transvenous biventricular pacing for heart failure: can the obstacles be overcome? Am J Cardiol. 1999;83(5B):136D-42.
14. Santoscoy R, Walters HL 3rd, Ross RD, Lyons JM, Hakimi M. Coronary sinus ostial atresia with persistent left superior vena cava. Ann Thorac Surg. 1996;61(3):879-82.
15. Jha NK, Gogna A, Tan TH, Wong KY, Shankar S. Atresia of coronary sinus ostium with retrograde drainage via persistent left superior vena cava. Ann Thorac Surg. 2003;76(6):2091-2.
16. Niebauer MJ, Daoud E, Williamson B, Man KC, Strickberger A, Hummel J et al. Atrial electrogram characteristics in patients with and without atrioventricular nodal reentrant tachycardia. Circulation. 1995;92(1):77-89.
17. Carneiro EF. A ativação do coração. In: O eletrocardiograma - 10 anos depois. Rio de Janeiro:Cervantes Editora;1997.
18. Warwickshire: General Practice Notebook - a UK medical encyclopedia on the World Wide Web; c2004. Disponível em: http://www.gpnotebook.co.uk [acessada em 1/12/2004].
19. Yee R, Pappone C, Maertens S et al. Clinical experience with over-the-wire left ventricular pacing lead for biventricular pacing in heart failure patients: multicenter report. Can J Cardiol. 2001;(suppl C):89C-288C.
20. Bergman RA, Afifi A, Miyauchi R. Coronary Sinus. In: Anson BJ, editor. Illustrated encyclopedia of human anatomic variation: Opus II: cardiovascular system: veins: head, neck, and thorax. 12ª ed. New York:McGraw-Hill;1966.
21. Lundinghausen M, Ohmachi N, Boot C. Myocardial coverage of the coronary sinus and related veins. Clin Anat. 1992;5:1-15.





 All scientific articles published at rbccv.org.br are licensed under a Creative Commons license
All scientific articles published at rbccv.org.br are licensed under a Creative Commons license