INTRODUÇÃO
A importância funcional dos músculos papilares foi acentuada em 1956, com os estudos de Rushmer et al. [1,2], demonstrando que, na fase inicial da sístole, os papilares promovem encurtamento do eixo longo dos ventrículos, aumentando o diâmetro da base, a tensão nas paredes e, conseqüentemente, a eficácia e ejeção sistólicas.
Lillehei et al. [3], em 1963, baseados nos postulados fisiológicos de Rushmer, realizaram as primeiras substituições da valva mitral preservando os músculos papilares e a cordoalha. Seus resultados confirmaram a importância funcional do aparelho subvalvar, mostrando redução significante da mortalidade operatória, nos pacientes operados pela equipe. Esses resultados, no entanto, foram prontamente contestados por Bjoerk et al. [4] e Rastelli et al. [5] em estudos independentes. Contudo, após os resultados de Carpentier [6] e impulsionadas pelos estudos de Miller et al. [7] e David et al. [8-11], as operações mitrais com preservação parcial ou total das cúspides e músculos papilares retornaram [12,13].
A papilopexia empregada por Lillehei et al. [3] consistiu na fixação da prótese tipo bola (Modelo Starr - Edwards), sem a retirada das cúspides ou na remoção da cúspide anterior, com preservação da posterior.
As primeiras operações procurando preservar também a contribuição de suporte do complexo papilar anterior foram realizadas e relatadas a partir de 1987 [14,15], com o cruzamento subvalvar da cordoalha, sendo um segmento de cúspide fixado ao topo do músculo papilar oposto, preservando ou não a cúspide posterior.
Miki et al. [16], em 1988, descreveram técnica de papilopexia com divisão central da cúspide anterior, em duas metades, fixando cada metade a sua comissura homolateral.
Buffolo et al. [17] e Puig et al. [18] empregaram com sucesso essa técnica na substituição valvar mitral em pacientes com insuficiência cardíaca importante, com melhora acentuada na recuperação funcional, sendo que este último grupo fixou os papilares com tração acima do nível do plano valvar. Bastos et al. [19] também empregaram variante da papilopexia de Miki et al. [16] na troca valvar, em pacientes com insuficiência cardíaca.
Com base nos resultados satisfatórios previamente relatados com emprego do cruzamento de cordas tendíneas e músculos papilares em cirurgias de trocas valvares mitrais [14,15], optou-se por nova sistematização de papilopexia cruzada [20], sendo objetivo do presente estudo descrever a sistematização da técnica, analisando seus resultados iniciais na preservação dos músculos papilares, em cirurgias de substituição valvar mitral e remodelamento ventricular, na insuficiência cardíaca (ICC).
MÉTODO
Com aprovação de Comissão de Ética Médica (Protocolo NPG1.14), foram estudados dez pacientes submetidos a cirurgia de troca valvar mitral, sendo sete (70%) do sexo masculino, com idade variável entre 15 e 75 anos (média de 44,4 ± 18,7 anos), portadores de disfunção valvar mitral reumática (50%), prolapso valvar mitral (10%) ou miocardiopatia dilatada e ICC (40%)- (Tabela 1).
Após atriotomia esquerda e adequada exposição da valva mitral, a cúspide anterior foi desinserida do anel e centralmente dividida, sendo cada metade, com seu complexo de cordas tendíneas, fixada à comissura oposta por sua extremidade medial (Figura 1).
Em seguida, foram implantadas próteses valvares mecânicas, modelo St Jude 27 em sete pacientes e bioprótese porcinas, modelo Labcor, em três casos (números 27, 29 e 31, respectivamente), fixadas ao anel valvar por meio de pontos separados, com redução do anel valvar mitral, para melhor remodelamento ventricular nos casos com ICC. As operações foram realizadas com circulação extracorpórea hipotérmica moderada, empregando-se cardioplegia sangüínea com potássio (25 mEq/l).
A função ventricular foi avaliada pelo método de Teichholz [21] por exames ultra-sonográficos realizados no pré-operatório e no trigésimo dia de pós-operatório. Para análise estatística, empregou-se o teste de Wilcoxon, com nível de significância de p<0,05.
RESULTADOS
Não ocorreram óbitos nem reoperações pós-operatórias na presente série.
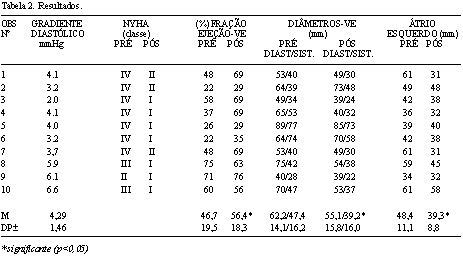
O cruzamento dos músculos papilares (Figura 2) não interferiu na função das próteses valvares implantadas, tampouco obstruiu via de saída do ventrículo esquerdo (Figuras 3A e 3B), possibilitando a recuperação funcional ventricular, com elevação da fração de ejeção do ventrículo esquerdo de 46,7 para 56,4 % (p<0,05), em média, nos períodos pré e pós-operatório hospitalar, respectivamente (Tabela 2).
COMENTÁRIOS
Encontra-se ainda aberta a discussão sobre a importância e eficiência da preservação de cordas tendíneas e músculos papilares na substituição valvar mitral, verificando-se conclusões diferentes mesmo em publicações mais recentes, como as de Yun et al. [22], concluindo por vantagens e de Dancini et al. [23], concluindo pela ausência de benefícios com o procedimento. Contudo, não existem, até o momento, estudos concluindo por piora dos resultados na preservação das estruturas de suporte valvar.
Assim, é possível entender-se que a preservação dos músculos papilares, independentemente do detalhe técnico adotado, favorece ou não interfere na recuperação da função sistólica ventricular, contudo, quando se analisa o potencial para remodelamento ventricular negativo pós-operatório, a papilopexia cruzada oferece suporte geométrico otimizado, reduzindo o deslocamento pendular das bases de cada papilar e, por conseguinte, da parede ventricular respectiva. Associada à redução do diâmetro do anel mitral, na miocardiopatia dilatada, com ICC, pode otimizar os benefícios do remodelamento ventricular.
Normalmente, com o fechamento das cúspides valvares, a fixação da cordoalha desloca-se para a parte central, de forma que, na diástole ou na sístole, a mesma pressão que projeta a cúspide para o átrio é transmitida às paredes ventriculares, contendo-as e tracionando-as. Quando os papilares são transferidos da posição central de fixação na borda livre da cúspide para a comissura homolateral, tornam-se perfeitamente paralelos à parede ventricular, permitindo deslocamento mais amplo da parede ventricular e favorecendo esfericidade indesejável. Também por este motivo, na presença de regurgitação valvar aórtica, fica muito maior o potencial de dilatação e remodelamento nocivo diastólico ventricular (Figura 4).
A papilopexia cruzada, com a implantação de cada metade da cúspide na comissura oposta (por sua extremidade medial ou lateral, para adaptação mais adequada da relação entre diâmetro do anel valvar e comprimento do segmento de cúspide com a respectiva cordoalha), encurta o ângulo de deslocamento das bases dos músculos papilares, garantindo melhor proteção contra a dilatação diastólica passiva ventricular (Figura 5).
Quando, por calcificação, fibrose acentuada ou infecção, não seja possível a preservação das cordas tendíneas para fixação dos papilares, o emprego de fitas ou cordas de pericárdio bovino fixado em glutaraldeído [24], ou de fios de PTFE [25], possibilita bons resultados.
A favor da papilopexia pontua também o princípio natural de preservação das estruturas anatômicas e de toda fisiologia possível dos órgãos operados. Além disto, a utilização da cúspide mitral posterior, reforçando o apoio das suturas no contorno posterior do anel valvar, onde é mais frágil, impõe-se de modo evidente, sempre que possível.
Discussão especial, entretanto, pode merecer a afirmação de importância dos músculos papilares nas substituições mitrais em corações muito dilatados. Nestes casos, a anatomia patológica ensina que a fixação dos músculos papilares posiciona-se na metade, ou até em nível mais alto, da cavidade ventricular, sem possibilidade de apoio à contração miocárdica, restringindo acentuadamente qualquer contribuição para a sístole cardíaca e a importância de sua preservação na operação de troca valvar mitral.
CONCLUSÃO
A presente investigação tem alcance prático definitivo prejudicado pela dificuldade natural de homogeneização da multiplicidade de aspectos inerentes ao quadro clínico dos pacientes e determinantes fisiopatológicas envolvidas, o que também justifica as diferenças de resultados e de interpretações a respeito na literatura mundial. Em análise geral, pode-se concluir que a técnica de papilopexia cruzada permitiu a substituição valvar mitral com recuperação funcional e remodelamento atrial e ventricular favorável e significantes, mesmo nos pacientes com quadro grave de ICC e miocardiopatia dilatada.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Rushmer RF. Initial phase of ventricular systole: asynchronous contraction. Am J Physiol. 1956;184(1):188-94.
2. Rushmer RF, Finlayson BL, Nash AA. Movements of the mitral valve. Circ Res. 1956;4(3):337-42.
3. Lillehei CW, Levy MJ, Bonnabeau Jr RC. Mitral valve replacement with preservation of papillary muscles and chordae tendineae. J Thorac Cardiovasc Surg. 1964;47(4):532-43.
4. Bjoerk VO, Bjoerk L, Malers E. Left ventricular function after resection of the papillary muscles in patients with total mitral valve replacement. J Thorac Cardiovasc Surg. 1964;48Oct.:635-9.
5. Rastelli GC, Tsakiris AG, Frye RL, Kirklin JW. Exercice tolerance and hemodynamic studies after replacement of canine mitral valve with and without preservation of chordae tendineae. Circulation. 1967;35(4 suppl.):I34-41.
6. Carpentier A. Cardiac valve surgery: "the French correction". J Thorac Cardiovasc Surg.1983;86(3):323-37.
7. Miller Jr. DW, Johnson DD, Ivey TD. Does preservation of the posterior chordae tendineae enhance survival during mitral valve replacement? Ann Thorac Surg. 1979;28(1):22-7.
8. David TE, Strauss HD, Mesher E, Anderson MJ, Macdonald IL, Buda AJ. Is it important to preserve the chordae tendinae and papillary muscles during mitral valve replacement? Can J Surg. 1981;24(3):236-9.
9. David TE, Uden DE, Strauss HD. The importance of the mitral apparatus in left ventricular function after correction of mitral regurgitation. Circulation. 1983;68(3pt2):II76-82.
10. David TE, Burns RJ, Bacchus CM, Druck MN. Mitral valve replacement for mitral regurgitation with and without preservation of chordae tendineae. J Thorac Cardiovasc Surg. 1984;88(5pt1):718-25.
11. David TE. Mitral valve replacement with preservation of chordae tendinae: rationale and technical considerations. Ann Thorac Surg. 1986;41(6):680-2.
12. Hansen DE, Cahill PD, DeCampli WM, Harrison DC, Derby GC, Mitchell RS et al. Valvular - ventricular interaction: importance of the mitral apparatus in canine left ventricular systolic performance. Circulation. 1986;73(3):1310-20.
13. Yagyu K, Matsumoto H, Asano K - Importance of the mitral complex in left ventricular contraction: an analysis of the results of mitral valve replacement with preservation of the posterior mitral complex. Thorac Cardiovasc Surg. 1987;35(3):166-71.
14. Gomes OM. Papilopexia para prevenção da degeneração miocárdica após substituição mitral. Arq Bras Cardiol. 1987; 49 (supl. 1):165
15. Pitchon M, David JPM, Caetano MC, Oliveira A, Gomes ES, Gomes OM. Técnicas de papilopexia em cirurgia da valva mitral. Coração. 1991;2(3):24-9.
16. Miki S, Kusuhara K, Ueda Y, Komeda M, Ohkita Y, Tahata T. Mitral valve replacement with preservation of chordae tendineae and papillary muscles. Ann Thorac Surg. 1988;45(1):28-34.
17. Buffolo E, Paula IM, Branco JNR, Carvalho ACC, Mantovani C, Caputi G et al. Tratamento da insuficiência cardíaca terminal através da correção da insuficiência mitral secundária e remodelação ventricular. Rev Bras Cir Cardiovasc. 2001;16(3):203-11.
18. Puig LB, Gaiotto FA, Oliveira Jr. JL, Pardi MM, Bacal F, Mady C et al. Mitral valve replacement and remodeling of the left ventricle in dilated cardiomyopathy with mitral regurgitation: initial results. Arq Bras Cardiol. 2002;78(2):224-9.
19. Bastos ES. Mitral valve replacement with subvalvar remodeling. In: 1st World Congress of the International Academy of Cardiovascular Sciences / Scientific Forum XIII; Belo Horizonte, Brazil;2003.
20. Gomes OM. Crossed papillopexy and surgical ventricular remodeling. In: Satellite Meeting of the International Society for Heart Research 2004. World Congress. Iguazu, Argentina;2004 Annals. p.14-22
21. Teichholz LE. In: Cardiel EA, Mortera C, Yuste P. Ecocardiografia: nuevas técnicas. Madrid:Ediciones Norma;1979.
22. Yun KL, Sintek CF, Miller DC, Pfeffer TA, Kochamba GS, Khonsari S et al. Randomized trial comparing partial versus complete chordal-sparing mitral valve replacement: effects on left ventricular volume and function. J Thorac Cardiovasc Surg. 2002;123(4):707-14.
23. Dancini JL, Pomerantzeff PM, Spina GS, Pardi MM, Giorgi MC, Sampaio RO et al. Troca valvar com preservação de cordas e plástica na cirurgia da insuficiência mitral crônica. Arq Bras Cardiol. 2004;82(3):235-42.
24. Gomes OM, Pitchon M, Barros MVL, Caetano MC, Oliveira NA, Gomes ES. Utilização de corda tendínea de pericárdio bovino em cirurgia da valva mitral. Coração. 1990;2(2):20-22
25. Frater RW, Vetter HO, Zussa C, Dahm M. Chordal replacement in mitral valve repair. Circulation. 1990;82(suppl IV):IV125-30.








 All scientific articles published at rbccv.org.br are licensed under a Creative Commons license
All scientific articles published at rbccv.org.br are licensed under a Creative Commons license