INTRODUÇÃO
A interposição de um enxerto para restabelecer a continuidade da aorta foi utilizada pioneiramente por Gross et al. (1), em 1949, para a correção da coarctação da aorta. Em 1951, Oudot (2) substituiu a bifurcação da aorta abdominal para tratar uma oclusão aorto-ilíaca e Dubost et al. (3), em 1952, reconstruíram o seguimento distal da aorta abdominal após a ressecção de um aneurisma. Nestes relatos pioneiros, assim como em outras reconstruções arteriais que se seguiram realizadas por estes e por outros cirurgiões, foram utilizados enxertos aórticos humanos preservados em solução salina balanceada nutriente a uma temperatura entre 1 e 4°C. Embora os resultados iniciais tenham sido muito satisfatórios, estes enxertos evoluíram para a dilatação aneurismática, e/ou para a trombose no intervalo de 1 a 3 anos.
Materiais sintéticos foram pesquisados experimentalmente e uma prótese confeccionada com material poroso foi utilizada com bons resultados em estudos experimentais relatados em 1952 por Voorhees et al. (5). Em 1954, Blakemore et al. (6) relataram pioneiramente o uso desta prótese vascular porosa confeccionada com Vinyon N em pacientes humanos. Durante a década de 1950, vários outros materiais com diferentes graus de biocompatibilidade foram investigados e utilizados experimentalmente e clinicamente, tais como Nylon, Ivalon, Teflon e Dacron. A introdução do princípio crimping proporcionou a manutenção da forma tubular das próteses vasculares sintéticas, mesmo quando fletidas, além de proporcionar uma elasticidade longitudinal. Dacron foi considerado o material de escolha para a confecção de próteses vasculares sintéticas, particularmente para a reconstrução da aorta e de vasos calibrosos. Estas próteses foram industrializadas, passando a ser disponíveis comercialmente nas configurações woven, knitted e velour, confeccionadas sem sutura e incorporando o princípio crimping (4, 7). Durante as últimas décadas, as próteses vasculares de Dacron têm sido utilizadas amplamente e com bons resultados tardios para a reconstrução da aorta torácica e abdominal, incluindo a reconstrução total da aorta ascendente e da valva aórtica, utilizando-se um conduto composto contendo uma prótese valvular aórtica (8-14). Entretanto, na correção de uma dissecção aórtica aguda, onde as paredes da aorta geralmente são delgadas e muito friáveis, ocorrem, com freqüência, complicações hemorrágicas severas, resultantes particularmente de sangramento ao nível da linha de sutura entre a parede friável da aorta e a prótese de Dacron, especialmente em sua configuração woven (8, 10, 13-15).
O pericárdio bovino preservado em glutaraldeído tem sido utilizado em nosso meio desde 1979 para alargamento da aorta ascendente (16) e posteriormente utilizado para a confecção de condutos valvados para a reconstrução total da aorta ascendente (17). O pericárdio é macio e flexível, o que facilita a realização da anastomose com uma aorta fina e friável, resultando em sutura hemostática com conseqüente redução das complicações hemorrágicas quando comparadas às próteses vasculares de Dacron (17).
Em 1987, foi desenvolvido um conduto de pericárdio bovino preservado em glutaraldeído para substituição vascular, incorporando o princípio crimping (18). Vários métodos foram utilizados para corrugar o pericárdio, visando à obtenção de um conduto biológico corrugado similar às próteses vasculares de Dacron e que mantivesse as características estruturais e funcionais do pericárdio. Estudos experimentais in vitro demonstraram integridade das fibras colágenas e da estrutura tissular, assim como integridade funcional e bioquímica do pericárdio submetido ao processo de corrugamento (18-20). Estudos experimentais, realizados em modelos animais no laboratório, demonstraram que estes condutos de pericárdio corrugado são de fácil manipulação, especialmente durante a realização das suturas, decorrentes do princípio crimping, que mantém a sua forma tubular. Foi demonstrado também que a superfície interna não é trombogênica, além das demais características do pericárdio, que é impermeável, não necessita pré-coagulação, não sangra, é macio e flexível, características que também facilitam a realização de anastomoses de boa qualidade técnica e hemostática (18-20).
Estes substitutos vasculares são industrializados por um laboratório de produtos biomédicos (Labcor Laboratórios, Belo Horizonte, M.G.) e disponíveis como condutos simples avalvulados (Figura 1) e como condutos compostos valvulados, contendo uma bioprótese aórtica porcina para substituição total da aorta ascendente e valva aórtica (Figura 2). São ainda confeccionados como condutos bifurcados para reconstrução da aorta abdominal distal incluindo as artérias ilíacas e/ou femorais (Figura 3). Os tubos de pericárdio bovino corrugado apresentam uma elasticidade longitudinal e a capacidade de manter o seu formato tubular e evitar o colabamento (efeito kinking), mesmo quando fletidos a 180°, de maneira similar às próteses vasculares corrugadas de Dacron (Figura 4).

Fig. 1 - Conduto de pericárdio bovino corrugado avalvular para reconstrução simples da aorta.

Fig. 2 - Conduto de pericárdio bovino corrugado contendo uma bioprótese porcina para reconstrução total da aorta ascendente.

Fig. 3 conduto de pericárdio bovino corrugado e bifurcado para reconstrução aorto-ilíaca e aorto-femoral.

Fig. 4 - O conduto de pericárdio bovino corrugado mantém a sua forma tubular mesmo quando fletido a 180o.
A experiência clínica inicial confirmou as vantagens demonstradas nos estudos experimentais em animais de laboratório com redução do sangramento intra e pós-operatório e ausência de complicações relacionadas ao substituto vascular nos primeiros anos de experiência e de seguimento clínico dos pacientes (19-23).
CASUÍSTICA E MÉTODOS
No período de outubro de 1989 a maio de 1997, 40 pacientes portadores de dissecção aórtica, aneurisma da aorta ou doença aórtica oclusiva foram submetidos a reconstrução da aorta utilizando-se condutos de pericárdio bovino corrugado processados pelo glutaraldeído. Dez destes pacientes foram admitidos em caráter de urgência devido a dissecção aórtica aguda tipo I em 6, dissecção aórtica aguda rota tipo III em 1 e dissecção aórtica aguda tipo I associada a infarto agudo do miocárdio resultante da dissecção da coronária esquerda em 1. Entre estes 10 pacientes havia também 1 paciente com aneurisma roto da aorta abdominal e 1 com aneurisma em expansão. Todos os 10 pacientes foram submetidos a operações de urgência. Os demais 30 pacientes foram admitidos para operações eletivas, incluindo a ectasia ânulo-aórtica, aneurisma da aorta ascendente, do arco aórtico, da aorta abdominal, aneurisma tóraco-abdominal, coarctação da aorta e doença oclusiva aorto-ilíaca (Tabela 1).
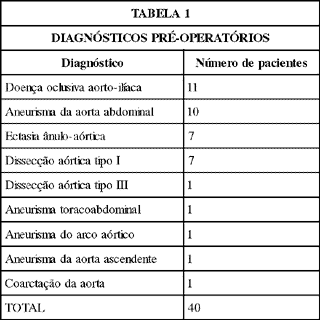
Os diagnósticos pré-operatórios foram confirmados pela aortografia em todos os pacientes submetidos a operações eletivas. Para os pacientes admitidos em caráter de urgência, o diagnóstico foi confirmado através da ecocardiografia e/ou da tomografia axial computadorizada. A idade variou entre 23 e 81 anos, com média de 56 anos. Havia 30 (75%) pacientes do sexo masculino e 10 (25%) do sexo feminino.
Procedimentos Cirúrgicos
A Tabela 2 mostra as operações realizadas nesta série de 40 pacientes. A esternotomia mediana foi utilizada para abordar os portadores de ectasia ânulo-aórtica, aneurisma da aorta ascendente e dissecção aórtica tipo I, utilizando-se circulação extracorpórea, hemodiluição, hipotermia sistêmica a 27°C e proteção miocárdica através de cardioplegia sangüínea ou cristalóide. A hipotermia profunda a 15°C com parada circulatória foi utilizada nos portadores de dissecção aórtica aguda envolvendo o arco-aórtico e de aneurismas do arco-aórtico. Condutos valvulados contendo uma bioprótese porcina foram utilizados para a substituição total da aorta ascendente e valva aórtica com reimplante das artérias coronárias, empregando-se a técnica descrita por Bentall & De Bono (9) em 8 pacientes e a técnica da Cabrol (10) em 1. O paciente com dissecção aórtica aguda tipo I e infarto agudo do miocárdio resultante da dissecção da coronária esquerda foi submetido a uma operação de Bentall & De Bono modificada, associando-se a revascularização miocárdica no território da coronária esquerda através de pontes de veia safena para a descendente anterior e para um ramo diagonal. Condutos avalvulados foram utilizados para a substituição da aorta ascendente quando a valva aórtica foi preservada. Nas dissecções aórticas, o falso lume foi obliterado proximalmente e distalmente com o uso da cola biológica (gelatina-resorcina polimerizada pelo formaldeído) e por pontos separados em U reforçados com tiras de pericárdio bovino por dentro e por fora da aorta. As anastomoses na aorta foram realizadas com sutura contínua utilizando-se fio de polipropileno 4-0. Foi também feita cerclágem da anastomose aórtica distal com a utilização de tira de pericárdio bovino.

A toracotomia póstero-lateral esquerda através do 4º espaço intercostal foi empregada em pacientes submetidos à reconstrução da aorta torácica descendente. Uma grande incisão associando uma toracotomia póstero-lateral com incisão abdominal extra-peritonial foi utilizada para abordar o aneurisma tóraco-abdominal. A laparotomia mediana foi a via de acesso empregada para abordagem das lesões da aorta abdominal e do segmento aorto-ilíaco. Os procedimentos sobre a aorta torácica descendente, aorta tóraco-abdominal e aorta abdominal foram realizados com simples pinçamento da aorta, empregando-se heparinização sistêmica.
As anastomoses foram sempre cuidadosamente inspecionadas à procura de pontos de sangramento, sendo utilizados pontos adicionais quando necessário. Subseqüentemente, as paredes do aneurisma foram usadas para recobrir o tubo de pericárdio corrugado, sempre que possível, e suturadas ao seu redor.
RESULTADOS
Resultados Imediatos
A mortalidade hospitalar (30 dias) foi de 8 (20%) pacientes e as causas de óbito estão ilustradas na Tabela 3. Sete destes pacientes foram operados de urgência devido a dissecção aórtica aguda tipo I em 6 e devido a dissecção aórtica aguda tipo III com rotura no espaço retropleural em 1. Este paciente evoluiu para óbito no pós-operatório em conseqüência de recidiva da dissecção aórtica em outros locais envolvendo toda a aorta, incluindo os ramos do arco aórtico e as artérias viscerais, assim como 1 paciente com dissecção aórtica aguda tipo I. Três pacientes com dissecção aórtica aguda tipo I foram a óbito devido ao baixo débito cardíaco, incluindo o paciente com infarto agudo do miocárdio resultante da dissecção da artéria coronária esquerda. Um paciente com dissecção aórtica aguda tipo I que apresentava uma aorta severamente doente e friável foi a óbito devido a hemorragia incontrolável ao nível das linhas de sutura. Outro paciente, também portador de dissecção aórtica aguda tipo I submetido a operação de Cabrol devido a dificuldade técnica na realização da técnica de Bentall & De Bono, evoluiu para a morte no pós-operatório em conseqüência de falência de múltiplos órgãos. O único paciente operado eletivamente que foi a óbito era portador de ectasia ânulo-aórtica e havia sido submetido a reconstrução total da aorta ascendente pela técnica de Bentall & De Bono; a causa da morte foi o baixo débito cardíaco.

A Tabela 4 mostra as 30 complicações intra-operatórias e pós-operatórias imediatas, que ocorreram em 18 pacientes e foram responsáveis pela morte de 8 deles. Hemorragia intra-operatória ocorreu em 6 pacientes, as quais foram controladas com facilidade através de suturas adicionais reforçadas com almofadas de pericárdio bovino em 4 deles. Devido a persistência do sangramento e formação de hematoma em um destes pacientes, foi necessário criar uma fístula entre o espaço paraprotético e o átrio direito após suturar a parede aneurismática da aorta ao redor do conduto de pericárdio bovino corrugado. Em 1 paciente com dissecção aórtica aguda tipo I submetido a reconstrução da aorta torácica ascendente o sangramento foi incontrolável, resultando em óbito por hemorragia.

Quatro pacientes complicados por baixo débito cardíaco evoluíram para óbito no pós-operatório imediato e 1 evoluiu para falência de múltiplos órgãos, que também resultou em morte no pós-operatório.
Três pacientes submetidos a reconstrução aorto-femoral apresentaram como complicação trombose de um dos ramos do conduto bifurcado, sendo submetidos a reoperação. Doença arterial difusa com um leito distal comprometido foi considerada a causa da trombose. A paciente com aneurisma tóraco-abdominal apresentou insuficiência renal aguda e paraplegia temporárias no pós-operatório imediato, evoluindo progressivamente para a recuperação sem seqüelas. O paciente com aneurisma do arco-aórtico desenvolveu pneumonia no pós-operatório imediato, infecção da ferida cirúrgica e septicemia, exigindo uma hospitalização prolongada, porém resultando em recuperação total e alta hospitalar.
Resultados Tardios
A avaliação tardia dos pacientes foi feita através do controle clínico ambulatorial, através de dados do prontuário hospitalar, do médico pessoal ou por contato telefônico. Este estudo coletou 128,4 pacientes-anos de seguimento total, correspondendo a um seguimento médio de 4 anos por paciente e um seguimento máximo de 8 anos e 4 meses. Os dados foram analisados através de métodos relacionados ao tempo, utilizando-se a distribuição exponencial e a análise atuarial pelo método de produto limite de Kaplan-Meier (24).
Ocorreram 5 óbitos tardios, correspondendo a uma mortalidade de 3,9% ± 1,7% por paciente-ano e as causas são mostradas na Tabela 5. Um paciente de 73 anos submetido a substituição da aorta abdominal infra-renal devido a aneurisma em expansão evoluiu para o óbito 3 meses após a operação devido a complicações metabólicas relacionadas a diabete e insuficiência renal crônica. Outro paciente também submetido a substituição do seguimento infra-renal da aorta abdominal devido a aneurisma, teve morte súbita 4 anos após a operação aos 74 anos de idade. Um paciente com 72 anos foi a óbito por pneumonia 6 meses após ser submetido a revascularização aorto-femoral devido a doença oclusiva aorto-ilíaca. Outro paciente também submetido a revascularização aorto-femoral foi a óbito após 5 anos em decorrência de doença coronária aos 61 anos de idade. O quinto paciente, também submetido a revascularização aorto-femoral teve infecção da prótese com formação de pseudo-aneurisma 15 meses após a operação; foi reoperado, houve recidiva da infecção e, após sucessivos procedimentos cirúrgicos, evoluiu para septicemia e óbito 20 meses após o procedimento inicial.

A curva de sobrevida atuarial para os 40 pacientes submetidos a reconstrução aórtica, calculada pelo método de Kaplan-Meier (24) está ilustrada no Gráfico 1 e mostra uma sobrevida atuarial (± erro padrão)I de 61,5% ± 9,2% em 9 anos, incluindo a mortalidade cirúrgica.

A Tabela 6 mostra as complicações tardias observadas entre os 32 pacientes que sobreviveram à operação, demonstrando que 4 das 6 complicações estavam relacionadas ao conduto de pericárdio e os pacientes necessitaram ser submetidos a reoperações. A incidência de complicações relacionadas ao conduto corrugado, assim como a incidência de reoperações foi 3,1% ± 1,6% por paciente-ano.

Trombose de um ramo de conduto bifurcado ocorreu 9 meses após a revascularização aorto-femoral por doença aorto-ilíaco-femoral oclusiva. A oclusão decorreu de um leito femoral distal difusamente lesado e da progressão da doença vascular periférica. Foi também observado, à reoperação, fibrose e crescimento de tecido autógeno na superfície interna do conduto do pericárdio ao nível da anastomose distal com a arterial femoral comum.
Infecção envolvendo o conduto de pericárdio bovino ocorreu em 3 pacientes submetidos a revascularização aorto-femoral. Esta infecção levou a uma degeneração secundária do conduto e resultou na formação de pseudo-aneurisma, correspondendo a uma incidência de 2,3% ± 1,4% por paciente-ano. Em 2 deles o pseudo-aneurisma desenvolveu-se próximo à anastomose distal entre o tubo de pericárdio e a artéria femoral 4 e 5 meses após a operação. No terceiro paciente um grande pseudo-aneurisma desenvolveu-se no espaço retro-peritonial próximo à anastomose proximal na aorta e bem distante da anastomose na artéria femoral. Os pseudo-aneurismas não se formaram nos locais das linhas de sutura nas anastomoses, mas eles resultaram de um processo degenerativo da parede do próprio conduto de pericárdio bovino resultante da infecção. Os achados cirúrgicos durante as reoperações mostraram um enfraquecimento da parede do tubo com rotura no local do pseudo-aneurisma e que se fragmentava durante a manipulação cirúrgica (Figura 5). Culturas do material removido à reoperação demonstraram a presença de Acinectobacter calcoaceticus no paciente que desenvolveu infecção próxima à anastomose femoral 4 meses após a operação e associação de Enterobacter sp e Streptococcus faecalis no paciente que também desenvolveu infecção próxima à anastomose femoral 5 meses após a operação. Bacillus sp foi identificado no paciente com pseudo-aneurisma próximo à anastomose na aorta e que ocorreu 15 meses após a operação.

Fig. 5 - Ramo infectado de um conduto de pericárdio bovino corrugado e bifurcado utilizado para reconstrução aorto-femoral, mostrando a degeneração resultante da infecção.
O exame histológico pela microscopia óptica mostrou uma reação inflamatória aguda com intensa atividade fagocitária e presença de macrófagos, leucócitos e neutrófilos.
As duas outras complicações tardias não estavam relacionadas ao conduto de pericárdio bovino. O paciente com 73 anos que evoluiu com insuficiência renal crônica após submeter-se a aneurismectomia da aorta abdominal em caráter de urgência, embora tenha recuperado a sua função renal, evoluiu para insuficiência renal crônica progressiva e veio a necessitar de hemodiálise.
COMENTÁRIOS E CONCLUSÕES
O pericárdio bovino processado em glutaraldeído tem sido utilizado amplamente na correção de lesões cardíacas congênitas, particularmente para o fechamento de comunicações interatriais e inter-ventriculares, para alargamento da via de saída do ventrículo direito e do tronco da artéria pulmonar, assim como para a confecção de um neo-septo atrial, a exemplo da operação de Mustard (25-27). Algumas complicações como retração, fibrose e calcificação têm sido relatadas quando o pericárdio é utilizado como um neo-septo atrial (26, 27), assim como quando submetido a baixa pressão (28), o que foi demonstrado experimentalmente (29). O pericárdio bovino também tem sido utilizado com bons resultados na confecção de condutos para a reconstrução da via de saída do ventrículo direito e do tronco da artéria pulmonar (28, 30). Entretanto, têm sido relatados alguns casos de retração, fibrose e estenose ao nível da anastomose distal, que também poderia estar relacionado à baixa pressão existente na artéria pulmonar (28).
O retalho de pericárdio bovino vem sendo utilizado por Braile et al. (16), desde 1979, para alargamento da aorta ascendente e, posteriormente, usado na confecção de tubos não corrugados para a reconstrução total da aorta ascendente (17). Bons resultados tardios foram relatados, assim como ausência de complicações tardias relacionadas ao conduto de pericárdio, tais como retração, fibrose e calcificação (31). Acredita-se que a alta pressão na aorta mantenha uma tensão sobre o pericárdio, evitando a sua retração, que poderia levar a fibrose e a calcificação, como já demonstrado experimentalmente em animais (29).
A maciez e a flexibilidade do pericárdio facilitam a realização de uma anastomose hemostática com uma aorta doente e as complicações hemorrágicas reduziram quando comparadas às próteses vasculares de Dacron (17, 32). A parede da aorta na presença de um aneurisma e, especialmente, de uma dissecção aguda é muito fina e friável e pode estar calcificada. A anastomose entre um tubo de Dacron woven espesso e duro com uma aorta doente, fina e friável pode ser difícil, resultando em sangramento na linha de sutura, que algumas vezes é incontrolável e pode ser fatal (8-10, 13-15). Uma prótese vascular intraluminal de Dacron sem sutura foi desenvolvida para evitar estas complicações hemorrágicas, sendo utilizada em casos selecionadas de dissecção aórtica (8). Foram descritos vários procedimentos cirúrgicos para o controle do sangramento intra-operatório. Uma das técnicas consiste na sutura da aorta aneurismática ao redor da prótese vascular, para controle da hemorragia nas linhas de sutura e do sangramento intersticial através da malha do Dacron (9). Outro procedimento se baseia na construção de uma fístula entre o espaço paraprotético e o átrio direito (10). Embora tais procedimentos possam ser necessários para promover a hemostasia na vigência de sangramento incontrolável, eles podem mascarar pontos importantes de sangramento, resultando em complicações tardias como pseudo-aneurismas e persistência da fístula aorta-átrio direito (15). A introdução da cola biológica representou uma contribuição importante na prevenção e controle da hemorragia intra-operatória (10). Outros procedimentos utilizados para minimizar o sangramento incluem o emprego de tubos de Dacron woven de baixa porosidade, diferentes técnicas de pré-coagulação e pré-cozimento, próteses impregnadas de colágeno e bandagem das anastomoses.
O conduto de pericárdio bovino corrugado é fácil de ser manipulado durante a operação. O corrugamento proporciona um tubo circular, que mantém a sua forma durante o procedimento e facilita a realização da anastomose. O pericárdio é muito macio e coapta muito bem nas linhas de sutura, resultando uma anastomose hemostática, mesmo na maioria das vezes em que foi anastomosado a uma aorta fina e friável. Isto é particularmente importante para o reimplante das artérias coronárias durante a substituição total da aorta ascendente. Outra vantagem é que este tubo de pericárdio tem uma superfície interna não trombogênica, é impermeável, não necessita pré-coagulação e não sangra. Sangramento ao nível das linhas de sutura ocorreu em 6 pacientes após a remoção da pinça da aorta, que foi facilmente controlado através de suturas adicionais ancoradas em almofadas de pericárdio em 4 deles. Em 2 pacientes o sangramento foi intenso e não se conseguiu controlar através de suturas adicionais.
Outra vantagem destes condutos é o baixo preço, quando comparado às próteses vasculares sintéticas.
Foi relatada menor incidência de infecção com o uso de condutos de pericárdio bovino não corrugados na substituição da aorta ascendente e do arco aórtico, quando comparados às próteses vasculares de Dacron (32). Acreditamos que isto possa estar relacionado à ação antimicrobiana do glutaraldeído absorvido pelo tecido pericárdico e não eliminado inteiramente pelos procedimentos de lavagem (33). Este glutaraldeído residual poderia manter uma atividade antimicrobiana durante a operação, assim como por várias horas e até dias após o implante do conduto (33).
Na presente experiência, ocorreram 3 casos de infecção envolvendo o conduto de pericárdio corrugado em pacientes submetidos a revascularização aorto-femoral e que evoluíram para a formação de pseudo-aneurisma. Em 2 deles a infecção e o pseudo-aneurisma estavam localizados próximos à anastomose distal na artéria femoral e ocorreram 4 e 5 meses após a operação. Estas infecções também poderiam estar relacionadas à eliminação do glutaraldeído residual do conduto de pericárdio, ao induzir reações citotóxicas aos tecidos circunvizinhos na região inguinal, onde o conduto é posicionado no tecido subcutâneo logo abaixo da pele. Estes efeitos tóxicos do glutaraldeído sobre qualquer tipo de célula poderia induzir a necrose no tecido subcutâneo, propiciando a proliferação de microorganismos (33). O terceiro paciente com diabete insulino-dependente desenvolveu infecção do conduto evoluindo para pseudo-aneurisma logo abaixo da anastomose aórtica 15 meses após a operação, o que não sugere estar relacionado a eventos intra e pós-operatórios imediatos. Nenhum caso de infecção ocorreu em pacientes nos quais a região inguinal não foi abordada, incluindo pacientes submetidos a revascularização aorto-ilíaca.
A degeneração da parede do tubo de pericárdio, com formação de pseudo-aneurisma, resulta de uma reação inflamatória aguda e presença de grande número de macrófagos e intensa atividade fagocitária por parte de células inflamatórias, incluindo leucócitos polimorfonucleares, macrófagos ativados e neutrófilos, que liberam enzimas proteolíticas, que provocam uma degeneração estrutural do colágeno, resultando na sua degradação e na fragmentação do pericárdio, e ainda a liberação de enzimas proteolíticas, tais como a colagenase e elastase por microorganismos presentes na infecção (34). Para minimizar este problema, os tubos de pericárdio bovino, especialmente os tubos bifurcados para reconstrução aorto-femoral devem ser bem lavados, seguindo as recomendações amplamente conhecidas de três lavagens separadas em 500 ml de solução salina durante 2 minutos cada e, em seguida, conservados em recipiente contendo solução salina até o momento do implante para reduzir a concentração de glutaraldeído residual ao mínimo (33).
A sobrevida atuarial em 9 anos livre de disfunção do conduto pela degeneração primária do tecido biológico foi de 100% e não foram observados casos de fibrose, calcificação ou dilatação aneurismática do tubo de pericárdio. Uma vez que o processo de corrugamento não altera as características funcionais e estruturais do pericárdio bovino, pode-se antecipar que os resultados tardios em seguimentos superiores a 10 anos para os condutos de pericárdio bovino corrugado devam ser similares aos resultados relatados para os tubos de pericárdio bovino não corrugados (31).
Infelizmente, o pericárdio bovino, assim como os demais xenoenxertos processados pelas técnicas atuais de preservação de tecido biológico pelo glutaraldeído, eventualmente evoluirão para a degeneração fibrocálcica, apesar dos bons resultados tardios obtidos até o presente.
AGRADECIMENTOS: O autor agradece ao Dr. Braulio R. G. M. Couto, pela colaboração no estudo estatístico e aos Drs. Carlos E. F. Starling e Adriana C. M. Magalhães, pelo estudo epidemiológico dos pacientes com infecção do conduto; e ao Prof. Eduardo A. Bambirra, pela realização do estudo histológico do pericárdio bovino.
REFERÊNCIAS BIBLIOGRÁFICAS
1 Gross R E, Bill Jr. A H, Peirce E C - Methods for preservation and transplantation of arterial grafts: observations on arterial grafts in dogs. Report of transplantation of preserved arterial grafts in nine human cases. Surg Gynecol Obstet 1949; 88: 689-701.
2 Oudot J - La greffe vasculaire dans les thromboses du carrefour aortic. Presse Med 1951; 59: 234-6.
3 Dubost C, Allary M, Oeconomos N - Resection of an aneurysm of the abdominal aorta: re-establishment of the continuity by a preserved human arterial graft with result after five months. Arch Surg 1952; 64: 405-8.
4 Lindenauer S M, Weber T R, Miller T A et al. - The use of velour as a vascular prosthesis. Biomed Eng 1976; 11: 301-6.
5 Voorhees Jr. A B, Jaretzki A, Blakemore A H - The use of tubes constructed from Vinyon "N" cloth in bridging arterial defects. Ann Surg 1952; 135: 332-6.
6 Blakemore A H & Voorhees A B - The use of tubes constructed from Vinyon "N" cloth in bridging arterial defects: experimental and clinical. Ann Surg 1954; 140: 324-34.
7 Lindenauer S M - The fabric vascular prosthesis. In: Rutherford R B, ed. Vascular surgery, Vol I, 3rd ed. Philadelphia: Saunders, 1989: 450-60.
8 Ablaza S G G, Ghosh S C, Grana V P - Use of a ringed intraluminal graft in the surgical treatment of dissecting aneurysm of the thoracic aorta. J Thorac Cardiovasc Surg 1978; 76: 390-6.
9 Bentall H & De Bono A - A technique for complete replacement of the ascending aorta. Thorax 1968; 23: 338-9.
10 Cabrol C, Pavie A, Mesnildrey P et al. - Long-term results with total replacement of the ascending aorta and reimplantation of the coronary arteries. J Thorac Cardiovasc Surg 1986; 91: 17-25.
11 Crawford E S & Crawford J L - Diseases of the aorta including an atlas of angiopraphic pathology and surgical technique. Baltimore: Williams & Wilkinns, 1984.
12 Crawford E S, Svenson L G, Coselli L S, Safi H J, Hess K R - Surgical treatment of aneurysm and/or dissection of the ascending aorta, transverse aortic arch, and ascending aorta and transverse aortic arch. J Thorac Cardiovasc Surg 1989; 98: 659-74.
13 Kouchoukos N T, Marshall W G, Wedige-Stecher T A - Eleven year experience with composite graft replacement of the ascending aorta and aortic valve. J Thorac Cardiovasc Surg 1986; 92: 691-705.
14 Miller D C, Stinson E B, Oyer P E et al. - Concomitant resection of ascending aortic aneurysm and replacement of the aortic valve. J Thorac Cardiovasc Surg 1980; 79: 388-401.
15 Kouchoukos N T - Aortic graft valve (composite) replacement at 20 years: wrap or no wrap? shunt or no shunt? Ann Thorac Surg 1989; 48: 615-6.
16 Braile D M, Ardito R V, Greco O T - Alargamento da raiz da aorta com "patch" de pericardio bovino preservado pelo glutaraldeído. Arq Bras Cardiol 1983; 41: 289-96.
17 Ardito R V, Santos J L V, Mayorquim R C et al. - Substituição completa da aorta ascendente e da valva aórtica com tubo valvulado de pericardio bovino. Rev Bras Cir Cardiovasc 1987; 2: 129-38.
18 Casagrande I S J, Puig L B, Salles C A, Ricardo O P - Tubo de pericardio bovino corrugado recoberto com Dacron: novo modelo de protese vascular. Rev Col Bras Cir 1988; 15 (Supl.): 153. (Resumo).
19 Salles C A, Puig L B, Casagrande I S, Vieira G L, Kalil R A - Crimped bovine pericardial conduit for arterial reconstruction. In: Annals of the 4th Annual Meeting of the European Association for Cardio-Thoracic Surgery. Naples, Italy: European Association for Cardio-Thoracic Surgery, 1990: A106 (Abstract).
20 Salles C A, Puig L B, Casagrande I S - Early experience with crimped bovine pericardial conduit for arterial reconstruction. Eur J Cardiothorac Surg 1991; 5: 273-9.
21 Salles C A - Crimped bovine pericardial conduit. In: Annals of the 2nd World Conference on Open Heart Surgery. Bombay, India: Association of Thoracic and Cardiovascular Surgeons of India, 1991: A52 (Abstract).
22 Salles C A, Ribeiro N A M, Kalil R A - Reconstrução arterial com tubo de pericardio bovino corrugado. In: Anais do 19º Congresso Nacional de Cirurgia Cardíaca. São Paulo, S.P.: Sociedade Brasileira de Cirurgia Cardiovascular, 1992: A34 (Resumo).
23 Salles C A, Ribeiro N A M, Kalil R A K - Reconstrução arterial com tubo de pericardio bovino corrugado. Rev Bras Cir Cardiovasc 1992; 7: 88-95.
[ Lilacs ]
24 Kaplan E L & Meier P - Nonparametric estimation from incomplete observations. J Am Stat Assoc 1958; 53: 457-81.
25 Crawford Jr. F A, Sade R M, Spinale F - Bovine pericardium for correction of congenital heart defects. Ann Thorac Surg 1986; 41: 602-5.
26 Cochran R P & McGouch E C - Bovine pericardium: a source of pulmonary obstruction in the Mustard procedure. Ann Thorac Surg 1987; 44: 552-3.
27 Bullaboy C A - Bovine pericardium: another cautionary note. Ann Thorac Surg 1989; 48: 743.
28 Fantini F A, Gontijo Fº B, Martins C - Emprego de condutos de pericárdio bovino na conecção ventriculo-arterial pulmonar; resultados tardios. Rev Bras Cir Cardiovasc 1996; 11: 161-7.
29 Gabbay S, Bortolotti U, Factors S, Shore D F, Frater M B - Calcification of implanted xenograft pericardium: influence of site and function. J Thorac Cardiovasc Surg 1984; 87: 782-7.
30 Moraes C R, Rodrigues J V, Gomes C A - Operação de Rasteli utlizando-se conduto valvulado de pericardio bovino: experiência inicial. Rev Bras Cir Cardiovasc 1988; 3: 84-92.
31 Braile D M, Leal J C, Zaiantchick M, Biagi P, Soares M J F - Replacement of the ascending aorta and aortic valve with bovine pericardium. In: Annals of the International Workshop Use of Pericardium in Cardiac Surgery. London, England: The Royal Society of Medicine, 1997: A40 (Abstract).
32 Gontijo B, Vrandecic M, Fantini F et al. - Replacement of the ascending aorta and aortic arch with bovine pericardial grafts. Eur J Cardiothorac Surg 1995; 9: 127-32.
33 Scott E M & Gorman S P - Glutaraldehyde. In: Block S S, ed. Disinfection, sterilization, and preservation. 4th ed. Philadelphia: Lea & Febiger, 1991: 596-614.
34 Vaudaux P E, Lew D P, Waldvogel F A - Host factors predisposing to and influencing therapy of foreign body infections. In: Bisno A L & Waldvogel F A, eds. Infections Associated with Indwelling Medical Devices. 2nd ed. Washington, D.C.: American Society for Microbiology, 1994: 1-29.












 All scientific articles published at rbccv.org.br are licensed under a Creative Commons license
All scientific articles published at rbccv.org.br are licensed under a Creative Commons license