INTRODUÇÃO
Desde a introdução da operação valvar a céu aberto, a dilatação do anel mitral, encontrada em todos os pacientes com regurgitação valvar mitral, tem sido tratada de modo conservador. Em 1956, vários cirurgiões, quase simultaneamente, começaram a corrigir' regurgitação mitral usando a plicatura anular, procedimento cirúrgico ainda utilizado nos dias atuais. Após observação das alterações anatômicas em pacientes com regurgitação mitral, Carpentier [1], o pai da cirurgia reconstrutora da valva mitral, preconizou várias técnicas para a correção da regurgitação mitral, incluindo a anuloplastia com anel protético. Desde então, vários Centros por todo mundo têm adotado suas diferentes técnicas com excelentes resultados. Antunes et al. [2], na África do Sul, difundiram, largamente, tal aplicação em pacientes reumáticos muito semelhantes aos nossos.
De 1979 a 1986, foram operados quase 100 pacientes empregando anel de Carpentier em nosso Serviço[3]. Ausência de dilatação da porção anterior do anel mitral entre os dois trígonos fibrosos foi observada em todos os casos. Entretanto, em todos os casos ela tem sido encontrada na parte posterior e mais intensamente no segmento próximo à comissura póstero-medial [4]. Desde 1987, temos empregado, rotineiramente, uma prótese aberta para a correção de regurgitação mitral na quase totalidade dos pacientes submetidos à operação conservadora [5]. Vários Centros, em nosso meio, têm utilizado esta prótese, incluindo Carvalho et al. [6], que a preconizaram também para a correção de regurgitação tricúspide em posição invertida. Em associação à anuloplastia, técnicas reconstrutoras foram também por nós desenvolvidas para a correção do prolapso valvar mitral secundário ao alongamento e/ou rotura de cordas tendíneas, as quais juntamente àquelas mundialmente conhecidas, da escola francesa, têm sido a base para o tratamento cirúrgico reconstrutor em nosso Serviço.
Devido ao grande número de pacientes com doença valvar reumática em nosso país, vários cirurgiões desenvolveram técnicas próprias de anuloplastia mitral, muito contribuindo para o desenvolvimento da operação reconstrutora.
Importante salientar que o empenho em preservar a valva mitral com regurgitação adquire importância ainda maior quando o paciente está na faixa etária abaixo dos 15 anos de idade, já que está sujeito a um número maior de reoperações.
ASPECTOS ANATÔMICOS DA VALVA MITRAL
Para que a contração da musculatura cardíaca resulte em trabalho efetivo, ela necessita de pontos de apoio. Estes são constituídos pelo esqueleto fibroso do coração, composto dos trígonos fibrosos direito e esquerdo e dos anéis das valvas aórtica, mitral, tricúspide e pulmonar. Todos os anéis valvares são completos, exceto o anel valvar mitral, cuja porção anterior, entre os trígonos fibrosos inexiste, sendo esta porção ocupada pelo anel completo da valva aórtica [7]. A valva mitral é, portanto, composta de um anel fibroso incompleto, uma porção do ventrículo esquerdo subjacente ao anel e por quatro válvulas (cúspides), sendo uma anterior e três posteriores (lateral, medial e posterior, propriamente dita). A anterior é uma válvula de excursão, enquanto as posteriores são de contenção. Compõem ainda esta estrutura as comissuras que nada mais são do que outras duas cúspides que correspondem ao ponto de união entre a cúspide anterior e as cúspides lateral e medial (posteriores).
Este conjunto de estruturas determina, num coração normal, que o anel tenha forma semelhante à de um rim, sendo o maior diâmetro aquele situado entre os dois trígonos e que corresponde à cúspide anterior. Este diâmetro não se alonga na presença de dilatação do ventrículo esquerdo. Qualquer que seja a causa da dilatação ventricular esquerda (miocardiopatia, miocardites ou sobrecarga de volume do ventrículo esquerdo) haverá uma dilatação do anel mitral no sentido ântero-posterior - como bem observou Carpentier em seus estudos - sendo mais pronunciada à direita, junto à comissura póstero-medial, como descrito por nós [8].
Durante a sístole ventricular, cordas tendíneas presas a músculos papilares impedem o prolapso das cúspides, evitando assim a regurgitação valvar. Cordas tendíneas também podem se sustentar na parede livre do ventrículo esquerdo, podendo ser marginais, intermediárias ou ditas estruturais, de acordo com a sua inserção na face ventricular das cúspides. O alongamento ou a rotura destas cordas levam sempre ao prolapso valvar com regurgitação mitral. Cordas estruturais, quando rotas, causam regurgitação mitral importante.
As cordas tendíneas são um feixe de fibras colágenas constituídas por um eixo central de colágeno denso, circundado por colágeno frouxo e elastina revestida por células endocárdicas. Histologicamente, apresentam constituição semelhante à das cúspides; predominam tecido colágeno, poucas fibras elásticas e musculares recobertas por células endoteliais e endocárdicas. Na região de inserção, a estrutura das cordas confunde-se de modo quase imperceptível com a das cúspides.
Os músculos papilares formam dois conjuntos, sendo um anterior e outro posterior. O conjunto anterior possui duas cabeças, uma anterior e outra posterior. O conjunto papilar posterior, comumente, possui três cabeças: uma anterior, uma intermediária e outra posterior. Cordas tendíneas conectadas à cabeça anterior são ancoradas à cúspide anterior, cordas conectadas à cabeça intermediária são ancoradas às comissuras e as cordas conectadas à cabeça posterior são ancoradas à cúspide posterior. O músculo papilar anterior recebe irrigação sangüínea da artéria descendente anterior e/ou da artéria circunflexa. O músculo papilar posterior é nutrido pela artéria coronária direita e/ou pela artéria circunflexa e seus ramos.
ANULOPLASTIA MITRAL
A anuloplastia consiste na correção da dilatação do anel valvar mitral. Deve ser o último procedimento da reconstrução valvar, após a atuação sobre as cúspides, cordas tendíneas e músculos papilares. Em nossa experiência, em apenas 15% dos pacientes ela constituiu-se em procedimento isolado.
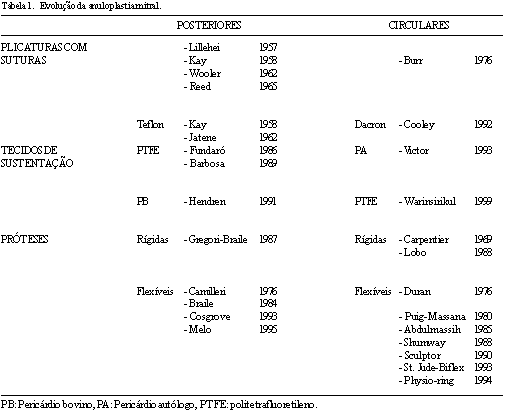
Tem sido realizada, ao longo dos anos, de várias maneiras. Para facilitar o entendimento dos vários métodos, propomos uma sistematização da anuloplastia de acordo com o material empregado (tecidos de sustentação, próteses, etc.) e forma de atuação (posterior, circular), a qual pode ser observada na Tabela 1.
Plicaturas
Foram as primeiras técnicas a serem utilizadas e, geralmente, consistem na plicatura do anel mitral junto às comissuras, fazendo com que as cúspides posteriores se aproximem da anterior, corrigindo assim a regurgitação central. Pode ser simétrica como proposto por Lillehei et al. [9] ou assimétrica como a de Kay et al. [10], Wooler et al. [11] e Reed et al. [12], sendo empregadas até os dias atuais. Nesta última, pontos são passados no anel mitral junto às comissuras, de modo a restringir mais intensamente o anel mitral posterior.
McGoon [13] e Merendino et al. [14], no início dos anos 60, desenvolveram técnicas para correção do prolapso das cúspides. A técnica deste último não deixa de ser uma anuloplastia, já que, após a ressecção da porção prolapsada da cúspide posterior, realiza-se a plicatura do anel mitral. Mais recentemente, outros autores como Burr et al. [15] propuseram a restrição circular de todo anel mitral, prática pouco adotada.
Com tecidos de sustentação
Nestes casos, tiras de materiais sintéticos como o Teflon, Dacron e o Politetrafluoretileno (PTFE) são aplicadas no anel posterior, jogando as cúspides posteriores de encontro à anterior (Kay et al. [10], Pomerantzeff et al. [16], Salati et al. [17], Barbosa et al. [18]), assim como Hendren et al. [19] vêm empregando barretes de pericárdio bovino em substituição aos materiais sintéticos.
A atuação em todo o perímetro do anel mitral foi preconizada por Cooley et al. [20] com anéis de Dacron e por Victor & Nayak [21] com pericárdio autólogo tratado com glutaraldeído. Recentemente, Warinsirikul et al. [22] têm utilizado anel confeccionado no ato operatório nas dimensões adequadas para o caso e consiste num cilindro de 3 mm2 de diâmetro, de PTFE, com um fio de aço no interior do tubo. Este fio é amarrado, inicialmente, e depois as bordas do tubo são aproximadas com pontos de seda, obtendo-se assim um "anel caseiro" com o formato ovóide, semelhante ao de Carpentier.
Com próteses posteriores
Rígidas
O anel por nós desenvolvido, denominado anel Gregori-Braile [4], trata-se de um hemi-anel fabricado em aço inoxidável 316 de grau médico, envolto por uma camada de borracha de silicone e, finalmente, coberto por veludo de Dacron. A ausência da haste anterior baseia-se no fato de que a dilatação do anel mitral raramente ou nunca se faz entre os trígonos fibrosos direito e esquerdo, espaço ocupado pelo anel fibroso da valva aórtica. Sua forma semicircular apresenta uma retificação na sua metade direita para corrigir a dilatação posterior do anel mitral, mais intensa à direita. Apresenta-se de vários tamanhos, podendo ser empregado inclusive em crianças pequenas. Os números variam de 24 a 36, de acordo com sua abertura máxima. A cada prótese corresponde um medidor metálico a ser utilizado, no ato operatório, para orientação na escolha do tamanho ideal. Esta deve se basear, exclusivamente, na distância entre as projeções das comissuras no anel mitral, não importando o diâmetro ântero-posterior. A maleabilidade do aço utilizado no anel protético permite pequenas modificações em sua abertura, podendo ser realizada manualmente, no ato operatório, para melhor ajuste de prótese ao anel mitral.
A fixação da prótese é feita com fios de poliéster 2-0 passados em "U" inicialmente no anel mitral e, em seguida, na parte externa do anel protético, sendo geralmente 7 a 8 fios. Com esta prótese, corrige-se a dilatação anular, evitando-se as manifestações tardias da estenose mitral em crianças e pacientes jovens, devido à restrição do crescimento normal do anel mitral, observada quando anuloplastias com próteses circulares são empregadas.
Flexíveis
Camilleri et al. [23] vêm empregando um redutor linear composto de um polímero de silicone revestindo uma trança de Dacron e dois fios de cobre, apresentando-se em segmentos de 20 centímetros. Não é extensível, nem compressível longitudinalmente para que uma redução almejada seja assegurada. É, no entanto, completamente flexível na sua largura para respeitar a fisiologia do anel mitral.
A prótese de pericárdio bovino descrita por Braile et al. [24] é constituída por um tubo de pericárdio bovino tratado em glutaraldeído, que tem no seu interior um fio de poliéster radiopaco. Desta forma, o conjunto, apesar de elástico, não está sujeito às deformações longitudinais. Uma vez implantada com pontos separados de poliéster 2-0 de trígono a trígono, a prótese molda o anel sem deformá-lo, aproximando a cúspide posterior da anterior de forma adequada.
Cosgrove et al. [25] desenvolveram um anel semicircular com haste maleável e com ajuste manual, de sorte a regular o grau de redução do diâmetro Ântero-posterior, após seu implante. A haste é confeccionada de veludo de poliéster para estimular sua rápida endotelização. É implantado com a ajuda de um molde rígido que é retirado apenas quando a prótese estiver totalmente fixa ao anel mitral.
Com próteses circulares
Rígidas
Carpentier [26] apresentou, em 1969, um anel circular rígido, feito em aço inoxidável revestido de Dacron que tem a forma de um rim, semelhante à do anel valvar mitral normal. Na implantação deste anel, aproximam-se as cúspides posteriores da anterior no sentido ântero-posterior, não interferindo no diâmetro transverso (intertrigonal). Tem o inconveniente de limitar o crescimento normal do anel mitral do paciente, quando empregado em crianças. Além disso, obstrução da via de saída do ventrículo esquerdo devido ao movimento anterior do anel mitral na sístole tem sido observada em indivíduos submetidos à anuloplastia para a correção de regurgitação mitral de etiologia degenerativa [27], fato raramente observado quando próteses abertas são empregadas. Importante destacar que, indubitavelmente, é a prótese mais utilizada no mundo.
Flexíveis
Dentre estes, o mais comumente empregado é o anel de Duran et al. [28]. Determina constrição circular uniforme do anel mitral dilatado, não poupando o diâmetro entre os trígonos fibrosos e exigindo criatividade do cirurgião para que a redução do diâmetro ântero-posterior seja adequada.
Uma série de próteses foram desenvolvidas visando aos ajustes na constrição anular após sua implantação, como as de Puig-Massana [29], Abdulmassih [30], Shumway [31], Sculptor [32] e St.Jude-Biflex [33], além de permitirem o movimento funcional de contração do anel mitral.
Mais recentemente, Carpentier et al. [34] criaram o Physio-ring, que apresenta o mesmo formato do anel original, sendo, transversalmente, flexível na sua porção posterior, permitindo contratilidade da correspondente parte do anel mitral. Sendo rígido, longitudinalmente, evita plicatura e efeito constritivo quando da fixação das suturas.
Faltam, no entanto, estudos randomizados, duplo cego e com número de casos adequados para se ter uma conclusão definitiva da superioridade, ou não, dos anéis flexíveis em relação aos rígidos.
CORREÇÃO DO PROLAPSO VALVAR MITRAL
O prolapso valvar mitral pode ser ocasionado pelo alongamento ou rotura de cordas tendíneas ou pela disfunção ou rotura dos músculos papilares secundária à regurgitação coronariana.
Em nosso meio, as causas mais freqüentes das lesões das cordas tendíneas são a febre reumática e a degeneração mixomatosa. Em ambas, o aparelho valvar mitral é globalmente acometido, especialmente as cordas tendíneas. Dependendo do grau de comprometimento e localização das cordas tendíneas lesadas, a técnica a ser empregada será adequada. O prolapso posterior, geralmente, é tratado com ressecção retangular parcial da cúspide posterior e plicatura do anel mitral neste nível, como proposto por Merendino et al. [14]. O prolapso anterior foi tratado inicialmente com ressecções cuneiformes da cúspide, ou mesmo plicaturas McGoon [13], métodos abandonados posteriormente, uma vez que limitam a mobilidade da cúspide anterior (cúspide de excursão). O mesmo problema não ocorre na ressecção da cúspide posterior (cúspides de contenção).
Vários procedimentos foram desenvolvidos para correção do prolapso da cúspide anterior.
Alongamento de cordas
Encurtamento de cordas com sepultamento intrapapilar, segundo Carpentier [1]
Esta técnica consiste em se realizar, inicialmente, uma incisão longitudinal na cabeça do músculo papilar. Em seguida, um fio polipropileno 5-0 laça por trás a corda ou o feixe de cordas alongadas, saindo com as agulhas inferiormente, nos bordos da incisão do músculo papilar. Na aplicação do nó, a corda é tracionada para baixo, corrigindo, assim, o alongamento das cordas. Quanto mais baixo saírem as agulhas, maior será o grau de encurtamento.
Encurtamento de cordas com sepultamento nas cúspides, segundo Gregori et al. [35]
Muito útil em crianças, em que os músculos papilares são delgados e o encurtamento fica difícil neste nível.
Um orifício de, aproximadamente, 2 mm é realizado na cúspide anterior da valva mitral, junto à inserção da corda tendínea alongada. Através deste orifício, a corda é tracionada para cima do plano valvar, observando-se o grau de encurtamento. Em seguida, procede-se a rafia da incisão com polipropileno 5-0, ao mesmo tempo em que a corda, já encurtada, é fixada em bloco, junto ao orifício da cúspide, corrigindo o prolapso. Mais de um encurtamento pode ser realizado ao longo da borda da coaptação da cúspide anterior. Recentemente, esta técnica foi empregada também para cúspide posterior em poucos casos, com resultado também satisfatório. A combinação das duas técnicas de encurtamento pode ser realizada no mesmo ato operatório.
Rotura de cordas tendíneas
Transferência de cordas da cúspide posterior para a anterior, segundo Carpentier et al. [36]
Trata-se de uma técnica empregada mundialmente. Uma parte da cúspide posterior da valva mitral, em contraposição à porção prolapsada da cúspide anterior, é destacada. Esta peça, contendo cúspide e cordas tendíneas, é deslocada para a borda livre da cúspide anterior, junto ao feixe de cordas rotas, sendo aí suturada com polipropileno 5-0, corrigindo-se, assim, o prolapso. As bordas da cúspide posterior seccionada são unidas por pontos separados de polipropileno 5-0, após plicatura do anel mitral no local correspondente.
Transferência parcial da valva tricúspide para a valva mitral, segundo Gregori et al. [37, 38]
Duas variantes técnicas são descritas. A primeira, mais freqüentemente empregada, consiste na remoção total da válvula posterior da valva tricúspide com todos os seus elementos, ou seja, cúspide, cordas tendíneas e músculo papilar. Esta peça é, então, translocada para a valva mitral com cordas rotas, suturando-se músculo papilar a músculo papilar, utilizando-se suturas em "U" de polipropileno 5-0, ancoradas em almofadas de Dacron. Em seguida, a cúspide do enxerto é suturada à borda livre da cúspide anterior da valva mitral, evitando-se deixar as cordas longas que poderiam manter o prolapso e, conseqüentemente, a regurgitação mitral. O mesmo cuidado deve ser tomado no caso oposto, deixando-se cordas curtas, com retração da cúspide anterior, impedindo-se a perfeita coaptação com a cúspide posterior.
O anel tricúspide é plicado com uma sutura em "U" de polipropileno 4-0, ancorada em almofadas de Dacron. A valva fica, portanto, bicúspide e uma eventual regurgitação tricúspide funcional presente é simultaneamente corrigida.
Prolapsos anteriores e posteriores da valva mitral podem ser corrigidos, simultaneamente, dividindo-se ao meio a cúspide do enxerto.
Criação de neocorda com retalho da cúspide anterior, segundo Gregori et al. [39]
Tem indicação, quase que exclusiva, para os casos com cúspide anterior da valva mitral, apresentando-se com área bem desenvolvida (degeneração mixomatosa ou síndrome de Barlow). Um retalho retangular do tecido da cúspide anterior é retirado, medindo, aproximadamente, 10 mm de comprimento por 2 mm de largura. Este retalho é destacado desde o anel até a borda livre da cúspide anterior, ficando preso apenas junto a esta última. Em seguida, é baixado à cabeça fibrosa do músculo papilar com rotura de cordas, onde é suturado, constituindo-se assim numa neocorda. Com o tempo, este retângulo de tecido se afila, adotando o aspecto de uma corda tendínea normal (fato observado em um paciente reoperado).
O orifício da cúspide anterior é suturado com pontos separados de polipropileno 5-0, ficando a cúspide anterior da valva mitral com área remanescente adequada.
Cordas artificiais
Materiais sintéticos e biológicos têm sido utilizados para a substituição das cordas tendíneas.
David et al. [40], desde 1985, têm empregado suturas de PTFE com excelente resultado a longo prazo em pacientes com prolapso da valva mitral secundário à rotura ou alongamento de cordas. Têm sido utilizadas por várias equipes em todo o mundo.
Frater et al. [41] introduziram o emprego de tiras de pericárdio bovino para a substituição das cordas. O temor com a calcificação deste tecido tem levado os cirurgiões a não utilizarem rotineiramente este método.
OUTRAS TÉCNICAS RECONSTRUTORAS
Retirada de calcificações localizadas, fenestração e secção de cordas retráteis, segundo Carpentier [1]
A restrição à mobilidade da cúspide é o resultado da fusão comissural, fusão de cordas, retração de cordas ou, mesmo, hipertrofia das mesmas. Pode-se realizar a secção de cordas secundárias, principalmente, aquelas oriundas da parede posterior do ventrículo esquerdo, propiciando, com isso, uma liberação da mobilidade da cúspide posterior, havendo assim melhor coaptação com a anterior. Também a fenestração das cordas, necessária algumas vezes em pacientes reumáticos, pela ressecção triangular das cordas fundidas, corrige a estenose subvalvar, melhorando também a mobilidade valvar. Calcificações localizadas podem ser retiradas com a ressecção em cunha da cúspide acometida, ou mesmo, pelo descolamento, das placas de cálcio.
Eventuais orifícios originados nestas membranas podem ser corrigidos com a colocação de um remendo de pericárdio autógeno, tratado ou não com glutaraldeído ou pericárdio bovino.
Utilização de retalhos de tecidos
Retalhos de pericárdio autólogo, tratado com glutaraldeído, têm sido empregados para o fechamento de orifícios pós-endocardite, ampliação das cúspides ou mesmo, substituição das mesmas, após ressecções de fibroses ou calcificações [42].
Substituição parcial da valva mitral por enxerto autólogo ou homólogo.
Hvass et al. [43] empregam técnica semelhante àquela desenvolvida por nós para casos de rotura de cordas da cúspide anterior, ou seja, a transferência parcial da valva tricúspide (cúspide posterior) para a valva mitral, somente que neste caso para substituição de parte da valva após ressecções de calcificações.
Revuelta et al. [44] demonstraram, em estudo experimental em carneiros, a viabilidade do emprego de homoenxertos criopreservados para a correção de lesões localizadas da valva mitral.
RESULTADOS EM CRIANÇAS
Entre maio de 1980 e novembro de 2001, 117 pacientes menores de 15 anos foram submetidos à operação conservadora da valva mitral. Todos portadores de regurgitação valvar mitral [45].
A idade variou de 1 a 15 anos, com média de 10 anos. Quarenta e três (36,8%) pacientes eram do sexo masculino e 74 (63,2%) do sexo feminino.
Oitenta e sete (74,4%) pacientes eram portadores de regurgitação mitral pura e 30 (25,6%) apresentavam estenose associada. A etiologia era a reumática em 95 (81,2%), congênita em 16 (13,7%), endocardite infecciosa em cinco (4,3%) e degeneração mixomatosa em um (0,9%) doente. Todos os pacientes encontravam-se nas classes funcionais III e IV.
Os pacientes foram operados com o auxílio de circulação extracorpórea (CEC) e hipotermia moderada, sendo a proteção miocárdica realizada com pinçamento intermitente da aorta, a qual era despinçada a cada 15 minutos. O tempo médio de CEC foi de 68 minutos (22-158 min) e o de isquemia do miocárdio, de 38 minutos (8-108 min).
Em todos os pacientes, o anel valvar mitral foi remodelado. Próteses ou tecidos de sustentação não foram utilizados em apenas sete pacientes. Em seis (5,1%) foram empregadas fitas de pericárdio bovino, em 35 (29,9%) anel de Carpentier e nos últimos 69 (59,0%) o anel de Gregori-Braile. A anuloplastia isolada foi realizada em 22 (18,8%) pacientes e em 95 (81,2%) houve necessidade de atuação sobre os folhetos da valva e/ou do aparelho subvalvar.
Sessenta e seis (56,4%) pacientes foram submetidos ao encurtamento de cordas alongadas, 30 (25,6%) à comissurotomia e/ou papilotomia, 11 (9,4%) à ressecção parcial da cúspide posterior, nove (7,7%) à ressecção da cúspide anterior, seis (5,1%) à plicatura da cúspide posterior, cinco (4,3%) à transposição de cordas, cinco (4,3%) à transferência de cordas, cinco (4,3%) à secção de cordas retráteis, quatro (3,4%) à sutura de orifícios nas cúspides e dois (1,7%) à retirada de cálcio da cúspide anterior.
Em associação foram realizados os seguintes procedimentos: plastia valvar tricúspide em seis (5,1%) pacientes, fechamento de comunicação interatrial em três (2,6%), ligadura do ducto arterial persistente em dois (1,7%), troca valvar aórtica em 10 (8,5%), plastia valvar aórtica em seis (5,1%), ressecção de anel fibroso subaórtico em um (0,9%), correção de canal atrioventricular em um (0,9%) e operação de Cox sem crioablação em um (0,9%).
Não ocorreram fenômenos tromboembólicos.
Cento e treze (96,6%) pacientes estão vivos, 104 (88,9%) com suas valvas nativas, 99 (84,6%) encontram-se em classe funcional I e II (NYHA).
A mortalidade hospitalar foi de um (0,9%) paciente com insuficiência cardíaca incontrolável e a tardia foi de três (2,6%), sendo que dois destes óbitos ocorreram em reoperações.
CONCLUSÃO
A operação reconstrutora da valva mitral possui um grande arsenal de técnicas e materiais que podem corrigir defeitos no anel valvar, cúspides ou aparelho subvalvar, permitindo o tratamento adequado da regurgitação valvar mitral e conseqüente preservação da valva. Assim, sempre que possível, deve ser a opção de escolha, com especial atenção e aplicabilidade nas crianças.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Carpentier A. Cardiac valve surgery: "the French correction". J Thorac Cardiovasc Surg. 1983;86(7):323-37.
2. Antunes MJ, Magalhães MP, Colsen PR, Kinsley RH. Valvuloplasty of rheumatic mitral valve disease: a surgical challenge. J Thorac Cardiovasc Surg. 1987;94(1):44-56.
3. Gregori Jr. F, Takeda RT, Silva SS, Façanha LA, Ribeiro IA, Aquino WF et al. Sete anos de experiência com plastia da valva mitral. Arq Bras Cardiol. 1986;47(4):269-74.
4. Gregori Jr. F, Silva SS, Baba K, Queiroz LT, Takeda R, Façanha LA et al. Um novo modelo de anel protético para pacientes com regurgitação valvar mitral: relato de dois casos. Arq Bras Cardiol. 1988;50(6):417-20.
5. Gregori Jr. F, Silva SS, Hayashi SS, Aquino W, Cordeiro C, Silva LR. Mitral valvuloplasty with a new prosthetic ring: analysis of the first 105 cases. Eur J Cardiothorac Surg. 1994;8(4):168-72.
6. Carvalho RG, Mulinari LA, Giublin PR, Mulaski JC, Silva Jr. AZ, Lopes LR et al. Emprego do anel de Gregori na posição invertida para o tratamento da regurgitação tricúspide: experiência inicial. Rev Bras Cir Cardiovasc. 1998;1(2):152-7.
7. Fortuna ABP. Anatomia cirúrgica da estenose mitral: aspecto valvar [Tese de livre docência]. Campinas: Universidade Estadual de Campinas, Faculdade de Ciências Médicas, 1983. 101p.
8. Gregori Jr. F. Cirurgia reparadora da valvar mitral com novo modelo de anel protético [Tese de doutorado]. São Paulo: Escola Paulista de Medicina, 1990. 90p.
9. Lillehei CW, Gott VL, DeWall RA, Varco RL. The surgical treatment of stenotic or regurgitant lesions of the mitral and aortic valves by direct vision utilizing a pump-oxygenator. J Thorac Surg. 1958;35(2):154-91.
10. Kay JH, Zubiate P, Mendez MA, Vanstrom N, Yokoyama T. Mitral valve repair for significant mitral insufficiency. Am Heart J. 1978;96(2):253-62.
11. Wooler GH, Nixon PG, Grimshaw VA, Watson DA. Experiences with the repair of the mitral valve in mitral incompetence. Thorax. 1962;17:49-57.
12. Reed GE, Tice DA, Clauss RH. Asymmetric exaggerated mitral annuloplasty: repair of mitral insufficiency with hemodynamic predictability. J Thorac Cardiovasc Surg. 1965;49:752-61.
13. McGoon DC. Repair of mitral insufficiency due to ruptured chordae tendineae. J Thorac Cardiovasc Surg. 1960;39:357-62.
14. Merendino KA, Thomas GI, Jesseph JE, Herron PW, Winterscheid LC, Vetto RR. The open correction of rheumatic mitral regurgitation and/or stenosis; with special reference to regurgitation treated by posteromedial annuloplasty utilizing a pump-oxygenator. Ann Surg. 1959;150(1):5-22.
15. Burr HB, Krayenbuhl C, Sutton M. The mitral plication suture: a new technique of mitral valve repair. J Thorac Cardiovasc Surg. 1977;73(4):589-95.
16. Pomerantzeff PMA, Azevedo JG, Ratti M, Moraes AV, Amato M, Grinberg M et al. Plastica da valva mitral em pacientes consecutivos: como é a evolução tardia? Avaliação clínica e ecocardiográfica. Rev Bras Cir Cardiovasc. 1991;6(2):63-79.
17. Salati M, Scrofani R, Santoli C. Posterior pericardial annuloplasty: a physiological correction? Eur J Cardiothorac Surg. 1991;5(5):226-9.
18. Barbosa G, Saadi, JF, Wender OCB, Saadi EK, Dussin LH, Silva RK. Plastia na regurgitação mitral reumática. Arq Bras Cardiol. 1997; 69(supl. 1). Resumo das comunicações. 53o. Congresso da Sociedade Brasileira de Cardiologia. São Paulo, 1997.
19. Hendren WG, Nemec JJ, Lytle BW, Loop FD, Taylor PC, Stewart RW et al. Mitral valve repair for ischemic mitral insufficiency. Ann Thorac Surg. 1991;52(6):1246-52.
20. Cooley DA, Baldwin RT, Wilansky S. A cost-effective Dacron annuloplasty ring. Ann Thorac Surg. 1993;56(1):185-6.
21. Victor S, Nayak VM. Truly flexible D-shaped autogenous pericardial ring for mitral annuloplasty. Ann Thorac Surg. 1993;56(1):179-80.
22. Warinsirikul W, Mokarapong P, Sangchote S, Chaiyodsilp S, Tanamai S. Midterm results of mitral valve repair with homemade annuloplasty rings. Ann Thorac Surg. 1999;68(1):63-6.
23. Camilleri LF, Miguel B, Bailly P, Legault BJ, D'Agrosa-Boiteux MC, Polvani GL et al. Flexible posterior mitral annuloplasty: Five-year clinical and doppler echocardiographic results. Ann Thorac Surg 1998;66(5):1692-7.
24. Braile DM, Ardito RV, Pinto GH, Santos JLV, Zaiantchick M, Souza DRS et al. Plástica mitral. Rev Bras Cir Cardiovasc. 1990;5(2):86-98.
25. Cosgrove DM, Arcidi JM, Rodriguez L, Stewart WJ, Powell K, Thomas JD. Initial experience with the Cosgrove-Edwards annuloplasty system. Ann Thorac Surg. 1995;60:495-504.
26. Carpentier A. La valvuloplastie: une nouvelle technique de valvuloplastie mitrale. Presse Med. 1969;77(7):251-3.
27. Schiavone WA, Cosgrove DM, Lever HM, Stewart WJ, Salcedo EE. Long-term follow-up of patients with left ventricular outflow tract obstruction after Carpentier ring mitral valvuloplasty. Circulation 1988;78(3 pt 2):I60-5.
28. Duran CG, Pomar JL, Revuelta JM, Gallo I, Poveda J, Ochoteco A et al. Conservative operation for mitral insufficiency: critical analysis supported by postoperative hemodynamic studies in 72 patients. J Thorac Cardiovasc Surg. 1980;79(3):326-37.
29. Murphy JP, Sweeney MS, Cooley DA. The Puig-Massana-Shiley annuloplasty ring for mitral valve repair: experience in 126 patients. Ann Thorac Surg. 1987;43(1):52-8.
30. Abdulmassih C. Um novo modelo de anel protético flexível. In: 16o Congresso Nacional de Cirurgia Cardíaca; 1989; São Paulo.
31. Shumway SJ, Gott VL, Reitz BH. A "designer" annuloplasty ring for patients with massive mitral annular dilatation. Ann Thorac Surg. 1988;46(6):695-6.
32. vanRijk-Zwikker GL, Mast F, Schipperheyn JJ. Comparison of rigid and flexible rings for annuloplasty of the porcine mitral valve. Circulation. 1990;82(5 suppl.):58-64.
33. Gorton ME, Piehler JM, Killen DA, Hoskins ML, Borkon AM. Mitral valve repair using a flexible and adjustable annuloplasty ring. Ann Thorac Surg. 1993;55(4):860-3.
34. Carpentier AF, Lessana A, Relland JIM, Belli E, Mihaileanu S, Berrebi AJ et al. The "physio ring": an advanced concept in mitral valve annuloplasty. Ann Thorac Surg. 1995;60(5):1177-86.
35. Gregori Jr. F, Silva S, Façanha L, Cordeiro C, Aquino W, Moure O. Preliminary results with a new technique for repairing elongated chordae tendineae of the anterior mitral valve leaflet. J Thorac Cardiovasc Surg. 1994;107(1):321-3.
36. Carpentier A, Relland J, Deloche A, Fabiani JN, D'Allaines C, Blondeau P et al. Conservative management of the prolapsed mitral valve. Ann Thorac Surg. 1978;26(4):294-302.
37. Gregori Jr. F. Transferência parcial da valva tricúspide para a valva mitral para o tratamento cirúrgico da regurgitação mitral por ruptura de cordas tendíneas [Tese de Professor Associado]. Londrina: Universidade Estadual de Londrina;1998. 78p.
38. Gregori Jr. F, Cordeiro CO, Croti UA, Hayashi SS, Silva SS, Gregori TE. Partial tricuspid transfer for repair of mitral insufficiency due to ruptured chordae tendineae. Ann Thorac Surg. 1999;68(5):1686-91.
39. Gregori Jr. F, Takeda R, Silva S, Façanha L, Meier MA. A new technique for repair of mitral insufficiency caused by ruptured chordae of the anterior leaflet. J Thorac Cardiovasc Surg. 1988;96(5):765-8.
40. David TE, Bos J, Rakowski H. Mitral valve repair by replacement of chordae tendineae with polytetrafluorethylene sutures. J Thorac Cardiovasc Surg. 1991;101(3):495-501.
41. Frater RW, Gabbay S, Shore D, Factor S, Strom J. Reproducible replacement of elongated or ruptured mitral valve chordae. Ann Thorac Surg. 1983;35(1):14-28.
42. Chauvaud S, Jebara V, Chachques J, el Asmar B, Mihaileanu S, Perier P et al. Valve extension with glutaraldehyde-preserved autologous pericardium: results in mitral valve repair. J Thorac Cardiovasc Surg. 1991;102(2):171-8.
43. Hvass U, Calliani J, Nataf I, Julliard JM, Vahanian A. Transfer of the posterior tricuspid leaflet and chordae for mitral valve repair. J Thorac Cardiovasc Surg. 1995;110(3):859-61.
44. Revuelta JM, Cagigas JC, Bernal JM, Val F, Rabasa JM, Lequerica MA. Partial replacement of mitral valve by homograft. An experimental study. J. Thorac Cardiovasc Surg. 1992;104(5):1274-9.
45. Cordeiro CO, Gregori Jr F, Gregori TEF, Murakami A, Abrão A. Resultados da operação reconstrutora da valva mitral em pacientes com idade inferior a 15 anos. Rev Bras Cir Cardiovasc. 2004;19:115-9.
 All scientific articles published at rbccv.org.br are licensed under a Creative Commons license
All scientific articles published at rbccv.org.br are licensed under a Creative Commons license